ГЛУТАМИНОВАЯ КИСЛОТА (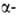 аминоглутаровая
к-та, Glu, E) HOOCCH2CH2CH(NH2)COOH, мол.
м. 147,13; бесцв. кристаллы. Для L-изомера т. пл. 247-249°С (с разл.);
аминоглутаровая
к-та, Glu, E) HOOCCH2CH2CH(NH2)COOH, мол.
м. 147,13; бесцв. кристаллы. Для L-изомера т. пл. 247-249°С (с разл.);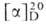 + 32° (1 г в 100 мл 6 н. НС1). Для D-изомера т. пл. 313оС (с
разл.); плохо раств. в воде и этаноле, не раств. в эфире. При 25 °С рКа
2,19
+ 32° (1 г в 100 мл 6 н. НС1). Для D-изомера т. пл. 313оС (с
разл.); плохо раств. в воде и этаноле, не раств. в эфире. При 25 °С рКа
2,19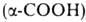 , 4,25
, 4,25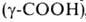 ,
9,67 (NH2); р/ 3,08.
,
9,67 (NH2); р/ 3,08.
По хим. св-вам Г. к.-типичная алифатич.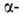 аминокислота.
При нагр. образует 2-пирролидон-5-карбоновую, или пироглутаминовую, к-ту,
с Си и Zn-нерастворимые соли. В образовании пептидных связей участвует
гл. обр.
аминокислота.
При нагр. образует 2-пирролидон-5-карбоновую, или пироглутаминовую, к-ту,
с Си и Zn-нерастворимые соли. В образовании пептидных связей участвует
гл. обр.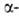 карбоксильная
группа, в нек-рых случаях, напр. у прир. трипептида глутатиона,-
карбоксильная
группа, в нек-рых случаях, напр. у прир. трипептида глутатиона,-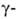 аминогруппа.
В синтезе пептидов из L-изомера наряду с
аминогруппа.
В синтезе пептидов из L-изомера наряду с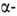 NН2-группой
защищают
NН2-группой
защищают карбоксильную
группу, для чего ее этерифицируют бензиловым спиртом или получают трет-бутиловый
эфир действием изобутилена в присут. к-т.
карбоксильную
группу, для чего ее этерифицируют бензиловым спиртом или получают трет-бутиловый
эфир действием изобутилена в присут. к-т. Группу
СООН остатков Г. к. в белках модифицируют так же, как у аспарагиновой
кислоты.
Группу
СООН остатков Г. к. в белках модифицируют так же, как у аспарагиновой
кислоты.
L-Г. к. встречается во всех организмах в своб. виде (в плазме крови
вместе с глутамином составляет ок. 1/3 всех своб. аминокислот)
и в составе белков. Р-ция L-Г. к. + + NН3 + АТФ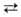 глутамин + АДФ + Н3РО4 (АДФ-аденозиндифосфат) играет
важную роль в обмене NH3 у животных и человека. В организме
декарбоксилируется до
глутамин + АДФ + Н3РО4 (АДФ-аденозиндифосфат) играет
важную роль в обмене NH3 у животных и человека. В организме
декарбоксилируется до аминомасляной к-ты, а через цикл трикарбоновых к-т превращ. в янтарную
к-ту. L-Г. к.-предшественник в биосинтезе орнитина и проли-на, участвует
в переаминировании при биосинтезе аминокислот, а также в транспорте ионов
К+ в центр. нервной системе.
аминомасляной к-ты, а через цикл трикарбоновых к-т превращ. в янтарную
к-ту. L-Г. к.-предшественник в биосинтезе орнитина и проли-на, участвует
в переаминировании при биосинтезе аминокислот, а также в транспорте ионов
К+ в центр. нервной системе.
Г. к.-кодируемая аминокислота, заменимая. Биосинтез L-Г. к. осуществляется
из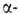 кетоглутаровой
к-ты: NH3 + НООСС(О)СН2СН2СООН + НАДФН
кетоглутаровой
к-ты: NH3 + НООСС(О)СН2СН2СООН + НАДФН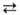 L-Г. к. + НАДФ, где НАДФН и НАДФ-соотв. восстановленная и окисленная формы
кофермента никотинамидадениндинуклеотидфосфата. В пром-сти ее получают
гл. обр. микробиол. синтезом из
L-Г. к. + НАДФ, где НАДФН и НАДФ-соотв. восстановленная и окисленная формы
кофермента никотинамидадениндинуклеотидфосфата. В пром-сти ее получают
гл. обр. микробиол. синтезом из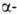 кетоглутаровой
к-ты. В спектре ЯМР L-Г. к. в D2O хим. сдвиги протонов (в м.
д.) у
кетоглутаровой
к-ты. В спектре ЯМР L-Г. к. в D2O хим. сдвиги протонов (в м.
д.) у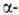 атома
С составляют 3,792, у
атома
С составляют 3,792, у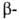 и
и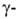 атомов-соотв.
2,136 и 2,537.
атомов-соотв.
2,136 и 2,537.
Мононатриевая соль Г. к., напоминающая по вкусу мясо, применяется в
пищ. пром-сти, соли Са и Mg-для лечения психич. и нервных заболеваний.
Мировое произ-во L-Г. к. ок . 270 тыс т/год (1982). В.В.Баев.


