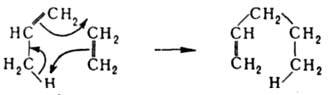
ЕНОВЫЕ РЕАКЦИИ (еновый синтез), присоединение олефинов или нек-рых др. соед. с двойной связью (енов). содержащих аллильный атом водорода, к ненасыщ. соед. (енофилам), сопровождающееся миграцией аллильного атома водорода и изменением положения двойной связи в еновом фрагменте, напр.:
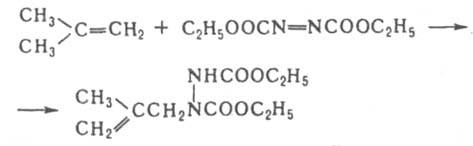
Е. р. родственны диеновому синтезу и легче всего происходят с электронообогащенными еновыми компонентами и электронодефицитными енофилами, напр.:
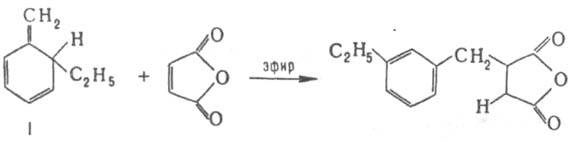
В случае, когда возможны неск. путей, р-ция идет с преимуществ. отрывом первичного атома водорода. Во мн. случаях диеновый синтез и Е. р. - конкурирующие процессы; строение аддукта определяется строением диеновой (еновой) компоненты. Так, напр., взаимод. соед. I с малеиновым ангидридом протекает только по схеме Е. р., несмотря на то что в молекуле имеется диеновая система с закрепленной цис-конфигурацией:
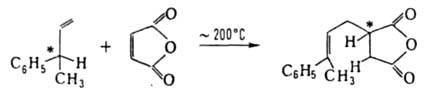
Е. р. термически разрешена как согласованный процесс с супраповерхностным взаимод. шести электронов: четырех от p-связей и двух от s-связи (см. Вудворда-Хофмана правило). Таким образом протекает р-ция оптически активного 3-фенил-1-бутена (звездочкой обозначен оптически активный атом С) с малеиновым ангидридом:
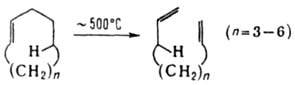
По аналогии с ретродиеновым синтезом известна также ретросновая р-ция, к-рая легче всего протекает в углеродных циклах средних размеров, напр.:
Е. р. используют в синтетич. орг. химии, напр., в химии стероидов. Лит.: Джилкрист Т., Сторр Р., Органические реакции и орбитальная симметрия, пер. с англ., М., 1976, с. 310; Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 222 Д. В. Давыдов.

Е. р. родственны диеновому синтезу и легче всего происходят с электронообогащенными еновыми компонентами и электронодефицитными енофилами, напр.:

В случае, когда возможны неск. путей, р-ция идет с преимуществ. отрывом первичного атома водорода. Во мн. случаях диеновый синтез и Е. р. - конкурирующие процессы; строение аддукта определяется строением диеновой (еновой) компоненты. Так, напр., взаимод. соед. I с малеиновым ангидридом протекает только по схеме Е. р., несмотря на то что в молекуле имеется диеновая система с закрепленной цис-конфигурацией:

Е. р. термически разрешена как согласованный процесс с супраповерхностным взаимод. шести электронов: четырех от p-связей и двух от s-связи (см. Вудворда-Хофмана правило). Таким образом протекает р-ция оптически активного 3-фенил-1-бутена (звездочкой обозначен оптически активный атом С) с малеиновым ангидридом:

По аналогии с ретродиеновым синтезом известна также ретросновая р-ция, к-рая легче всего протекает в углеродных циклах средних размеров, напр.:

Е. р. используют в синтетич. орг. химии, напр., в химии стероидов. Лит.: Джилкрист Т., Сторр Р., Органические реакции и орбитальная симметрия, пер. с англ., М., 1976, с. 310; Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 222 Д. В. Давыдов.


