КАРНИТИН (от лат. саrо, род. падеж carnis - мясо) (бетаин 3-гидрокси-4-триметиламиномасляной к-ты, витамин Вт)
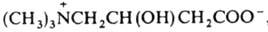 , мол. м. 161,21; бесцв. кристаллы; т.пл. L- и D, L-K. соотв. 142 и 197-212 °С (с разл.); для L-K. [a]D20 —30,9° (вода); гигроскопичен, хорошо раств. в воде и этаноле. При взаимод. с водным р-ром щелочи легко дегидратируется с образованием бетаина 4-триметиламинокротоновой к-ты (кротонобетаин).
К. присутствует в тканях животных (в значит. кол-вах в мышцах), бактериях и растениях (биол. активностью обладает только L-K.). Нек-рые насекомые (напр., личинки мучного червя Tenebrio molitor), для к-рых К. - фактор роста, не синтезируют его (для них К. - витамин). Высшие животные способны синтезировать К. из L-лизина в результате многостадийного процесса. Для них К. - кофермент, участвующий в переносе остатков жирных к-т через мембраны из цитоплазмы в митохондрии.
В цитоплазме жирные к-ты с длинной цепью находятся в активир. состоянии в виде тиоэфиров с коферментом А [KoSC(O)R; KoS - остаток кофермента A (KoSH), C(O)R -ацил жирной к-ты], к-рые не способны проникать через мембраны. На наружной стороне мембраны под влиянием встроенной в мембрану карнитин-ацилтрансферазы I катализируется р-ция:
, мол. м. 161,21; бесцв. кристаллы; т.пл. L- и D, L-K. соотв. 142 и 197-212 °С (с разл.); для L-K. [a]D20 —30,9° (вода); гигроскопичен, хорошо раств. в воде и этаноле. При взаимод. с водным р-ром щелочи легко дегидратируется с образованием бетаина 4-триметиламинокротоновой к-ты (кротонобетаин).
К. присутствует в тканях животных (в значит. кол-вах в мышцах), бактериях и растениях (биол. активностью обладает только L-K.). Нек-рые насекомые (напр., личинки мучного червя Tenebrio molitor), для к-рых К. - фактор роста, не синтезируют его (для них К. - витамин). Высшие животные способны синтезировать К. из L-лизина в результате многостадийного процесса. Для них К. - кофермент, участвующий в переносе остатков жирных к-т через мембраны из цитоплазмы в митохондрии.
В цитоплазме жирные к-ты с длинной цепью находятся в активир. состоянии в виде тиоэфиров с коферментом А [KoSC(O)R; KoS - остаток кофермента A (KoSH), C(O)R -ацил жирной к-ты], к-рые не способны проникать через мембраны. На наружной стороне мембраны под влиянием встроенной в мембрану карнитин-ацилтрансферазы I катализируется р-ция:
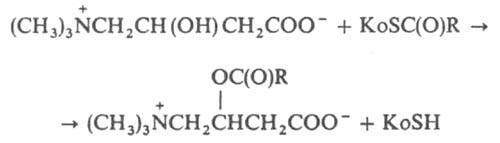
Образующийся ацил-К. переносится с участием фермента карнитин-ацилкарнитин-транслоказы к внутр. стороне мембраны. Здесь с участием карнитин-ацилтрансферазы II (также встроенной в мембрану) происходит ресинтез KoSC(O)R, а освободившийся К. вновь переносится через периплазматич. пространство к внеш. стороне мембраны. Т. обр., с помощью К. жирные к-ты оказываются в сфере действия окислит. ферментов, локализованных внутри митохондрий. Перенос этих к-т через внутр. перегородки митохондрий, по-видимому, осуществляется по аналогичному механизму. Хим. синтез К. осуществляют обычно из эпихлоргидрина последовательно обработкой триметиламином и цианидом щелочного металла, гидролизом образовавшегося нитрила 3-гидрокси-4-триметиламиномасляной к-ты до К. Расщепление на оптич. изомеры проводят на стадии получения нитрила. Др. путь синтеза L-K. - стереоспецифич. восстановление с помощью дрожжей октил-3-оксо-4-хлорбутирата до L-октил-3-гидрокси-4-хлорбутирата, взаимод. последнего с триметиламином и послед. гидролизом образующегося продукта. К. применяют в медицине в виде D, L- и L-карнитинхлорида в качестве нестероидного анаболич. ср-ва. Лит.: Ленинджер А., Основы биохимии, пер. с англ., т. 2, М., 1985, с. 554-55; Carnitine biosynthesis and function. Minisymposium, St. Louis, Missouri, June 4, 1981, "Federal. Proceeding", 1982, v. 41, № 12, p. 2840-42. A. M. Юркевич.
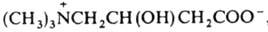 , мол. м. 161,21; бесцв. кристаллы; т.пл. L- и D, L-K. соотв. 142 и 197-212 °С (с разл.); для L-K. [a]D20 —30,9° (вода); гигроскопичен, хорошо раств. в воде и этаноле. При взаимод. с водным р-ром щелочи легко дегидратируется с образованием бетаина 4-триметиламинокротоновой к-ты (кротонобетаин).
К. присутствует в тканях животных (в значит. кол-вах в мышцах), бактериях и растениях (биол. активностью обладает только L-K.). Нек-рые насекомые (напр., личинки мучного червя Tenebrio molitor), для к-рых К. - фактор роста, не синтезируют его (для них К. - витамин). Высшие животные способны синтезировать К. из L-лизина в результате многостадийного процесса. Для них К. - кофермент, участвующий в переносе остатков жирных к-т через мембраны из цитоплазмы в митохондрии.
В цитоплазме жирные к-ты с длинной цепью находятся в активир. состоянии в виде тиоэфиров с коферментом А [KoSC(O)R; KoS - остаток кофермента A (KoSH), C(O)R -ацил жирной к-ты], к-рые не способны проникать через мембраны. На наружной стороне мембраны под влиянием встроенной в мембрану карнитин-ацилтрансферазы I катализируется р-ция:
, мол. м. 161,21; бесцв. кристаллы; т.пл. L- и D, L-K. соотв. 142 и 197-212 °С (с разл.); для L-K. [a]D20 —30,9° (вода); гигроскопичен, хорошо раств. в воде и этаноле. При взаимод. с водным р-ром щелочи легко дегидратируется с образованием бетаина 4-триметиламинокротоновой к-ты (кротонобетаин).
К. присутствует в тканях животных (в значит. кол-вах в мышцах), бактериях и растениях (биол. активностью обладает только L-K.). Нек-рые насекомые (напр., личинки мучного червя Tenebrio molitor), для к-рых К. - фактор роста, не синтезируют его (для них К. - витамин). Высшие животные способны синтезировать К. из L-лизина в результате многостадийного процесса. Для них К. - кофермент, участвующий в переносе остатков жирных к-т через мембраны из цитоплазмы в митохондрии.
В цитоплазме жирные к-ты с длинной цепью находятся в активир. состоянии в виде тиоэфиров с коферментом А [KoSC(O)R; KoS - остаток кофермента A (KoSH), C(O)R -ацил жирной к-ты], к-рые не способны проникать через мембраны. На наружной стороне мембраны под влиянием встроенной в мембрану карнитин-ацилтрансферазы I катализируется р-ция:

Образующийся ацил-К. переносится с участием фермента карнитин-ацилкарнитин-транслоказы к внутр. стороне мембраны. Здесь с участием карнитин-ацилтрансферазы II (также встроенной в мембрану) происходит ресинтез KoSC(O)R, а освободившийся К. вновь переносится через периплазматич. пространство к внеш. стороне мембраны. Т. обр., с помощью К. жирные к-ты оказываются в сфере действия окислит. ферментов, локализованных внутри митохондрий. Перенос этих к-т через внутр. перегородки митохондрий, по-видимому, осуществляется по аналогичному механизму. Хим. синтез К. осуществляют обычно из эпихлоргидрина последовательно обработкой триметиламином и цианидом щелочного металла, гидролизом образовавшегося нитрила 3-гидрокси-4-триметиламиномасляной к-ты до К. Расщепление на оптич. изомеры проводят на стадии получения нитрила. Др. путь синтеза L-K. - стереоспецифич. восстановление с помощью дрожжей октил-3-оксо-4-хлорбутирата до L-октил-3-гидрокси-4-хлорбутирата, взаимод. последнего с триметиламином и послед. гидролизом образующегося продукта. К. применяют в медицине в виде D, L- и L-карнитинхлорида в качестве нестероидного анаболич. ср-ва. Лит.: Ленинджер А., Основы биохимии, пер. с англ., т. 2, М., 1985, с. 554-55; Carnitine biosynthesis and function. Minisymposium, St. Louis, Missouri, June 4, 1981, "Federal. Proceeding", 1982, v. 41, № 12, p. 2840-42. A. M. Юркевич.


