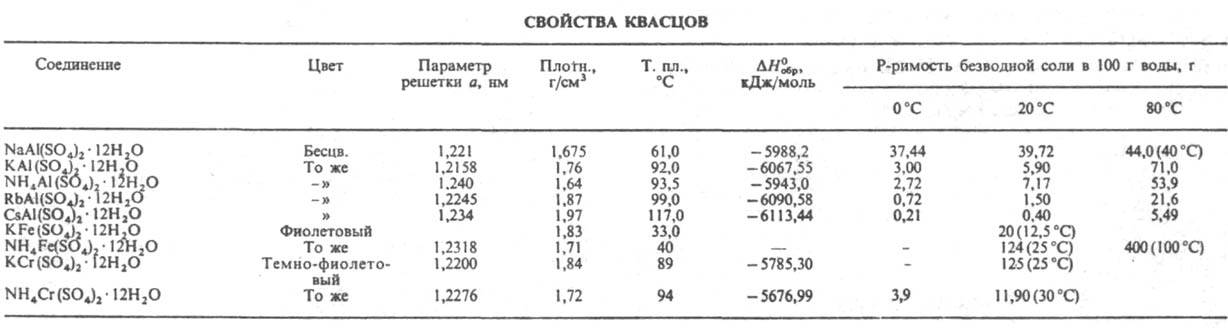
КВАСЦЫ, кристаллогидраты двойных сульфатов состава МIМIII(SО4)2.12Н2О [или M2SO4.M2III(SO4)3.24H2O], где М1 - однозарядный катион -Na+, K+, Rb+, Cs+, NH+4, Тl+, CH3NH3+ и др., МIII - трехзарядный катион - А13+, Сг3+, Fe3+, Ga3+, In3 и др. Существуют также селенатные квасцы аналогичного состава MIMlII(SeO4)2.12Н2О. Двухзарядные катионы образуют т. наз. псевдоквасцы сходного с К. состава, но иной структуры, напр. FeSO4 .A12(SO4)3324Н2О. Известно неск. десятков разл. К. Способность к образованию К., их устойчивость возрастают по мере увеличения радиуса М+ и уменьшения радиуса М3+ (при сходной внеш. электронной оболочке). При этом более сильное влияние на св-ва К. оказывает природа М+ . Так, алюмолитиевые К., в отличие от алюминиевых К. с более крупными катионами (Na+, К+ и др.), при т-ре 20-25°С не образуются, а м.б. получены лишь при т-ре ок. -2°С. Катион А13+ (ионный радиус 0,057 нм) дает К. с Li+, Na+ , К+ , NH+4, Rb+, Cs+, в то время как In3+ (0,092 нм) - только с Cs+, Rb+ и NH4 в виде метастабильных фаз. У К., содержащих один и тот же катион М3+ , в ряду Na, К, NH4, Rb, Cs р-римость в воде падает, а т-ра плавления и их термич. устойчивость увеличиваются (см. табл.). К. легко выделяются из водных р-ров в виде больших октаэдрич. кристаллов с кубич. решеткой (z = 4, пространств, группа РаЗ). Известны три структурные разновидности К. - a, b и g, отличающиеся друг от друга ориентацией тетраэдров SO4 по отношению к М+ и нек-рыми др. признаками. Эти различия обусловлены размером однозарядного катиона. b-К. содержат относительно большие катионы (Cs+, CH3NH3+), a-катионы меньшего размера (К+, Rb+), единств, представитель g-К. NaAl(SO4)2.12H2O. В кристаллич. структурах всех К. катионы М3+ и М+ координируют по 6 молекул воды. В Р-К. в координац. сферу М+ входят также 6 атомов кислорода анионов SO2-4. a- и b-К. образуют твердые р-ры между собой, g-К. твердых р-ров с др. К. не дают. К. обладают вяжущим и кислым вкусом, их водные р-ры имеют кислую р-цию вследствие гидролиза. При нагр. К. плавятся в кристаллизац. воде, затем дегидратируются в две или неск. стадий с образованием промежут. кристаллогидратов, напр. NaAl(SO4)2.6H2O, KAl(SO4)2.8Н2О, KAl(SO4)2.2H2O. Конечные продукты дегидратации - безводные, или "жженые", К.
В природе встречаются алюмокалиевые К., алюмонатpиевые (минерал сольфатерит) и алюмоаммониевые (минерал чермигит). Алюмокалиевые К. получают обжигом алунита K2SO4.A12(SO4)3.Аl(ОН)3 с послед. выщелачиванием сульфатов К и Аl водой и кристаллизацией К. из р-ра, а также разложением нефелина серной к-той при нагревании с послед. взаимод. полученного р-ра с К.Сl. Алюмонатриевые К. производят при переработке нефелина или упариванием р-ров сульфатов Na и Аl. Железо-аммониевые К. получают кристаллизацией из р-ра, содержащего сульфаты Fe(III) и аммония, хромово-калиевые К. - восстановлением К2Сr2О7 в разб. H2SO4 щавелевой к-той, спиртом и др. Практич. применение находят в осн. алюминиевые, хромово-калиевые и железо-аммониевые К.- как дубильные в-ва в кожевенной пром-сти (хромовые и алюминиевые К.), протравы при крашении тканей (хромовые, алюминиевые и железные К.), для проклеивания бумаги в бумажной пром-сти, в качестве кровоостанавливающего и прижигающего ср-ва в медицине (алюминиевые К.), коагулянтов при водоочистке и очистке сточных вод (алюминиевые и железные К.), реактива в фотографии (железные и хромовые К.), реагента в аналит. химии для обнаружения ионов NCS-, PO3-4, AsO3-4 и др. (железные К.). Лит.. Позив М. Е., Технология минеральных солей, 4 изд., ч. 1, Л.. 1974, с. 566, 613. 632, 635, 640. 653; Крисанова Л. П., "Ж. неорг. химии". 1986. т. 31, в 6, с. 1551 55 В. П. Данилов.


