ЛИПОКСИГЕНАЗЫ (полиненасыщ. жирных к-т : кислород оксидоредуктазы), ферменты класса оксидоредуктаз, катализирующие окисление полиненасыщ. жирных к-т (ПНЖК), молекулы к-рых содержат 1,4-циc, цис-пентадиеновый фрагмент, с одновременным перемещением двойной связи:
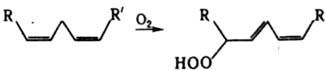
С меньшей скоростью окисляют сложные эфиры ПНЖК, в т. ч. глицериды и эфиры стеринов, полиненасыщ. спирты и алкилгалогениды. Способны также катализировать окисление ПНЖК, содержащих более двух двойных связей, с образованием дигидропероксидов с тремя сопряженными двойными связями в молекуле. Л. обнаружены в вегетативных частях, плодах (соя, пшеница, горох, томаты и др.) и клубнях (картофель) растений, а также в клетках крови (лейкоциты, тромбоциты, ретикулоциты) и тканях животных (легкие, почки, селезенка, сердце и др.). Локализованы преим. в водной фазе цитоплазмы (цитозоле) клеток; предполагают, что нек-рые Л. могут существовать в мембраносвязанной форме. Молекула Л. (мол. м. 60 тыс.-100 тыс.) у животных и нек-рых растений состоит из одной полипептидной цепи. Содержит в активном центре ион негемового Fe3+ (восстановленная форма Л. - неактивна); исключение - нек-рые грибы, в к-рых обнаружены гемсодержащие Л. У растений оптим. каталитич. активность фермента при рН 6-7 или 9-10 (в зависимости от источника и изофермента) у животных - при рН 7,4-7,8; рI обычно 5-6. Изучена аминокислотная последовательность Л. соевых бобов и, частично, ретикулоцитов. Активаторы Л. - гидропероксиды ПНЖК (в малых концентрациях), при гемолизе к-рых в активном центре Fe2+ окисляется до Fe3+. В анаэробных условиях Л. проявляют "пероксидазную" активность, восстанавливая гидропероксиды ПНЖК в присут. субстрата до гидроксипроизводных. Ингибиторы Л. - хелаты металлов, нек-рые антиоксиданты, флавоноиды, ацетиленовые аналоги субстратов и гидроксипроизводные ПНЖК. Накопление продуктов ферментативной р-ции (гидропероксидов ПНЖК) вызывает необратимую инактивацию Л. вследствие окисления серосодержащих аминокислот, входящих в состав активного центра фермента. Биол. роль Л. окончательно не установлена. Предполагают, что Л. могут участвовать в деструкции биомембран, напр. при трансформации ретикулоцитов в эритроциты. В лейкоцитах и др. типах клеток Л. участвуют в биосинтезе лейкотриенов и липоксинов (сопряженных тетраенов). Лит.: Ланкин В. 3., "Укр. бioхiм. журнал". 1984. т. 56, № 3. с. 317-31 Ланкин В. 3. [и др.], "Биохимия". 1985, т. 50, в. 11. с. 1894-1900; Vliegenthart J.,Veldink С., в кн.: Free radicals in biology, v. 5. N. Y. U 1982, p. 29-64; Hansson G., Malmsten C., Radmark О., в кн.: Prostaglandins and related substances, Amst. N.Y. Oxf., 1983. p. 127-69. В. З. Ланкин.
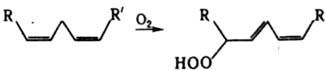
С меньшей скоростью окисляют сложные эфиры ПНЖК, в т. ч. глицериды и эфиры стеринов, полиненасыщ. спирты и алкилгалогениды. Способны также катализировать окисление ПНЖК, содержащих более двух двойных связей, с образованием дигидропероксидов с тремя сопряженными двойными связями в молекуле. Л. обнаружены в вегетативных частях, плодах (соя, пшеница, горох, томаты и др.) и клубнях (картофель) растений, а также в клетках крови (лейкоциты, тромбоциты, ретикулоциты) и тканях животных (легкие, почки, селезенка, сердце и др.). Локализованы преим. в водной фазе цитоплазмы (цитозоле) клеток; предполагают, что нек-рые Л. могут существовать в мембраносвязанной форме. Молекула Л. (мол. м. 60 тыс.-100 тыс.) у животных и нек-рых растений состоит из одной полипептидной цепи. Содержит в активном центре ион негемового Fe3+ (восстановленная форма Л. - неактивна); исключение - нек-рые грибы, в к-рых обнаружены гемсодержащие Л. У растений оптим. каталитич. активность фермента при рН 6-7 или 9-10 (в зависимости от источника и изофермента) у животных - при рН 7,4-7,8; рI обычно 5-6. Изучена аминокислотная последовательность Л. соевых бобов и, частично, ретикулоцитов. Активаторы Л. - гидропероксиды ПНЖК (в малых концентрациях), при гемолизе к-рых в активном центре Fe2+ окисляется до Fe3+. В анаэробных условиях Л. проявляют "пероксидазную" активность, восстанавливая гидропероксиды ПНЖК в присут. субстрата до гидроксипроизводных. Ингибиторы Л. - хелаты металлов, нек-рые антиоксиданты, флавоноиды, ацетиленовые аналоги субстратов и гидроксипроизводные ПНЖК. Накопление продуктов ферментативной р-ции (гидропероксидов ПНЖК) вызывает необратимую инактивацию Л. вследствие окисления серосодержащих аминокислот, входящих в состав активного центра фермента. Биол. роль Л. окончательно не установлена. Предполагают, что Л. могут участвовать в деструкции биомембран, напр. при трансформации ретикулоцитов в эритроциты. В лейкоцитах и др. типах клеток Л. участвуют в биосинтезе лейкотриенов и липоксинов (сопряженных тетраенов). Лит.: Ланкин В. 3., "Укр. бioхiм. журнал". 1984. т. 56, № 3. с. 317-31 Ланкин В. 3. [и др.], "Биохимия". 1985, т. 50, в. 11. с. 1894-1900; Vliegenthart J.,Veldink С., в кн.: Free radicals in biology, v. 5. N. Y. U 1982, p. 29-64; Hansson G., Malmsten C., Radmark О., в кн.: Prostaglandins and related substances, Amst. N.Y. Oxf., 1983. p. 127-69. В. З. Ланкин.


