МИЦЕЛЛИРНЫЙ КАТАЛИЗ,
ускорение хим. р-ций в присут. мицелл ПАВ. Обусловлен гл. обр. изменением
концентрации реагирующих в-в при переходе реагентов из р-ра в мицеллы; для р-ций
с участием диссоциирующих частиц существенно также влияние мицелл ПАВ на константу
скорости и сдвиг равновесия диссоциации молекул реагентов. Наиб. корректное
описание М. к. дает псевдодвухфазная модель, к-рая рассматривает наблюдаемую
скорость р-ции как сумму скоростей процессов в фазе р-рителя (воде или неводной
среде в случае "обращенных" мицелл) и мицелляр-ной псевдофазе, характеризуемых
соотв. константами скоростей kb и km. Распределение
реагентов А, В, ... между мицеллами и р-рителем описывается с помощью констант
РА = [А]m/[А]b, PB
= [В]т/[В]b, где [A] m-
концентрация в-ва в мицеллярной псевдофазе, [А]b- концентрация
в-ва в р-рителе. Для наиб. распространенного случая бимолекулярной р-ции типа
А + В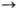 продукты,
наблюдаемая константа скорости второго порядка равна
продукты,
наблюдаемая константа скорости второго порядка равна
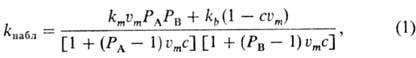
где um- молярный
объем ПАВ, с - концентрация ПАВ в мицеллярной форме, т.е. общая концентрация
ПАВ минус критич. концентрация мицеллообразования. Из ур-ния (1) следует, что
даже при отсутствии к.-л. влияния мицелл на константу скорости р-ции (km
= kb)они могут вызывать значит. ускорение вследствие концентрирования
реагентов в мицеллярной псевдофазе при РА>> 1 и РB>>1.
Напр., в случае ацилирования салицилальдоксима n-нитрофенило-вым эфиром
триметилуксусной к-ты в присут. бромида цетилтриметиламмония (БЦТА) при рН 7,2
резкое увеличение скорости (см. рис.) происходит при достижении критич. концентрации
мицеллообразования (ККМ) ПАВ, а затем kнабл проходит через
максимум. Величина ускорения при оптим. концентрации БЦТА-2.103
раз; константы Р для р-ции этого типа равны 102-103.
Связывание реагентов с
мицеллами для ионных в-в
определяется величинами их гидрофобного и электростатич. взаимодействия. Если
один из реагентов связывается сильно, а другой распределен равномерно между
обеими фазами (РА >> 1, РB = 1), то
М. к. проявляется только при условии km > kb. Это
же условие необходимо для ускорения р-ций первого порядка. Если один из реагентов
преим. находится в мицеллярной псевдофазе, а другой-в водной (РА>>1,
РB<<1), то при km пр.= kb
будет наблюдаться ингибирование за счет разделения реагентов. Ур-ние (1) не
пригодно для описания кинетики быстрых р-ций, происходящих за времена, близкие
к временам жизни молекул реагентов внутри мицелл ПАВ, напр. тушения фотолюминесценции.
Для этих систем развиты спец. подходы, учитывающие статистич. распределение
молекул реагентов между мицеллами.
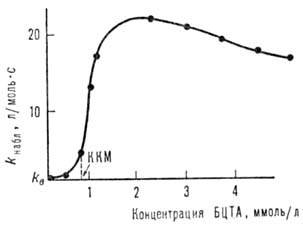
Зависимость kна6л
от концентрации бромида цетилтриметиламмония (БЦТА) при ацилировании салицилальдоксима
n-нитрофениловым эфиром триметилуксусной к-ты (kB =
= 0,012 л/моль.с).
М.к. применяют для разнообразных
хим. р-ций: эмульсионная полимеризация, идущая с участием молекул мономера,
включенного в мицеллы ПАВ; нуклеоф. замещение, напр. гидролиз сложных и простых
эфиров, амидов, шиф-фовых оснований; электронный перенос с участием орг. и неорг.
окислит.-восстановит. пар; замещение лиганда в комплексах металлов; фото- и
радиационно-хим. р-ции и др. Важное самостоят. направление - изучение каталитич.
ф-ций ферментов, включенных в обращенные мицеллы ПАВ. М. к. исследуется также
как модель ферментативного катализа. В этом отношении особенно перспективны
т. наз. функцион. мицеллы, образованные молекулами ПАВ с ковалентно связанными
каталитически активными группами.
Лит.: Мицеллообразование,
солюбилизация и микроэмульсии, под ред. К. Миттел, пер. с англ., М., 1980; Fendler
J.H., Fendler E.J., Catalysis in miccllar and macromolecular systems, N.Y.,
1975; Thomas J.K., "Chem. Rev.", 1980, v. 80, №4, p. 283-99; Turro
N.J., Graetzel M., Braun A.M., "Angew. Chem., Intern. Ed.", 1980,
v. 19, p. 675-96. A.K. Яцимирский.


