ТЕТРАФТОРЭТИЛЕН (перфторэтилен,
мономер М-4) CF2=CF2, мол.м. 100,02; бесцв. газ без запаха;
т.пл. - 131,15 °С, т. кип. - 76,3 °С;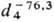 1,519;
tкрит 33,30С, pкрит 3,95
МПа, dкрит 0,572 г/см3; давление пара (МПа): 0,0822
(-80°С), 1,004 (-20°С), 1,776 (0°С), 2,928 (20 °С), 3,691 (30
°С); DHисп 16,53 кДж/моль (при -76,3°С), — 659,5
кДж/моль; р-римость в воде 0,018% по
1,519;
tкрит 33,30С, pкрит 3,95
МПа, dкрит 0,572 г/см3; давление пара (МПа): 0,0822
(-80°С), 1,004 (-20°С), 1,776 (0°С), 2,928 (20 °С), 3,691 (30
°С); DHисп 16,53 кДж/моль (при -76,3°С), — 659,5
кДж/моль; р-римость в воде 0,018% по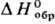 массе
(20 °С), в тетрафтордибромэтане 10,7% (-20°С) и 2,7 (20 °С).
массе
(20 °С), в тетрафтордибромэтане 10,7% (-20°С) и 2,7 (20 °С).
По хим. св-вам - типичный
фторолефин. В атмосфере О2 разлагается до СО2 и
CF4, при 200 °С начинается термич. разложение, при 600-800°С
образуются продукты внедрения дифторкарбена и димеризации:
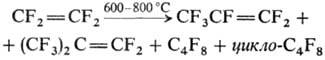
В контролируемых условиях
(О2, УФ облучение) окисляется до малостабильного тетрафторэтиленоксида;
последний легко превращ. в олигомерные перфторполи-эфиры:
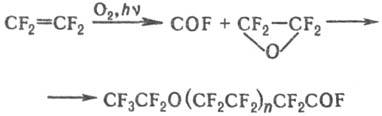
В присут. источников аниона
F- в апротонных полярных р-рителях образует реакционноспособный пентафторэтиль-ный
анион, к-рый легко подвергается дальнейшим превращениям:
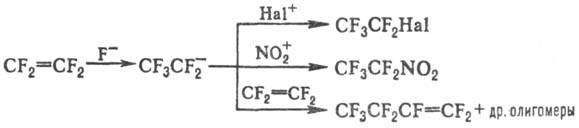
Т. реагирует с олефинами
с образованием циклических и линейных продуктов; с нитрозоалканами образует,
как правило, смесь оксазетидинов и линейных сополимеров:
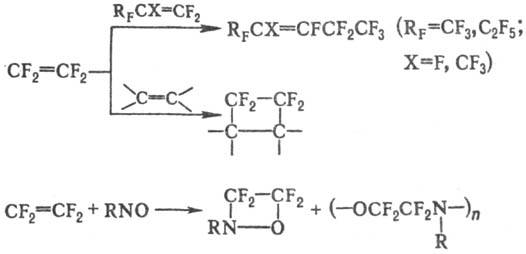 '
'
Взаимодействие Т. с перфторбром-
и перфториодалка-нами, перфтордиалкилдисульфидами, пероксисульфурил-фторидом
и др. приводит к соответствующим теломерам, напр.:
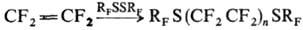
RF - перфторалкил
Полимеризация и сополимеризация
Т. приводит к хемо-и термостойким полимерам.
В пром-сти Т. получают
пиролизом CF2HCl при 700-800 °С. Др. способы: пиролиз политетрафторэтилена,
перфторциклобутана, трифторметана или др. фторорг. соед.; высокотемпературное
гидрирование CF2ClCF2Cl или CF2Cl2;
дегалогенирование тетрафтордихлор(дибром)этана с помощью металлов; декарбоксилирование
солей пер-фторпропионовой к-ты.
Применяют Т. для получения
разл. полимеров (напр., тефлона) и сополимеров (напр., с этиленом, гексафторпро-пиленом,
нитрозоперфторалканами и др. олефинами), инертных тяжелых жидкостей и смазок,
а также ряда фторорг. соединений.
При вдыхании Т. поражает
слизистые оболочки верх. дыхат. путей и легочной ткани, вызывает функцион. расстройства
центр. нервной системы. ПДК рабочей зоны производств. помещений 30 мг/м3,
макс. разовая ПДК в воздухе населенных мест 6 мг/м 3 (класс опасности
4).
Т.-горючий и взрывоопасный
газ. При соприкосновении с открытым пламенем или нагретыми пов-стями разлагается
с образованием высокотоксичных продуктов. КПВ 13,4-46,4% по объему. При хранении
в жидкой фазе способен к спонтанной взрывообразной полимеризации.
Лит.: Рахимов А.
И., Химия и технология фторорганических соединений, М., 1986; Промышленные фторорганические
продукты. Справочник, Л., 1990. И. И. Крылов.


