ТИЕНОТИОФЕНЫ, мол.
м. 140,23. Различают таено [2,3-b]тиофен (тиофтен, ф-ла I), тиено[3,2-b]тиофен
(II), тиено[3,4-b]тиофен (III) и тиено[3,4-с]тиофен (IV), к-рый
известен в виде тетрафенилпроизводного.
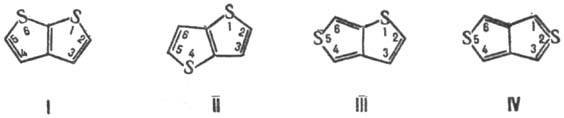
Все Т.-легкоплавкие кристаллы
с запахом нафталина. Для I т. пл. 6,25-6,5 °С. т. кип. 224-226 °С (пикрат,
т. пл. 137-138°С), m 3,86·10-30 Кл·м; для II т. пл. 56°С,
т. кип. 221-224 °С (пикрат, т.пл. 145 °С); для III т.пл. 7-7,5 °С,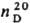 1,6905, m 3,42·10-30 Кл·м; для 1,3,4,6-тетрафенилтиено[3,4-с]тиофена
т.пл. 245-248°С; для 1H,3H-тиено[3,4-с]тиофена т.пл.
61-62°С.
1,6905, m 3,42·10-30 Кл·м; для 1,3,4,6-тетрафенилтиено[3,4-с]тиофена
т.пл. 245-248°С; для 1H,3H-тиено[3,4-с]тиофена т.пл.
61-62°С.
Т. представляют собой 10p-электронные
ароматич. системы. По хим. св-вам они во многом аналогичны тиофе-ну. Дают
индофениновую р-цию с изатином, под действием конц. к-т полимеризуются. По реакц.
способности в р-циях замещения, окисления и гидрогенолиза соед. I и II в неск.
раз превосходят незамещенный тиофен. В I и II наиб. активны положения 2 и 5,
в III-положения 4 и 6.
Метилзамещенные соед. I
и П обнаружены в сырой нефти. Осн. способ получения Т. и их производных-циклизация
соед. алифатич. или тиофенового ряда, напр. циклизация a,b-бифункциональнозамещенных
производных тиофена:
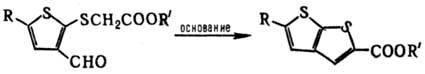
Соед. I и II используют
в синтезе метиновых красителей.
Лит.: Litvinov V.
P., Goldfarb Ya. L., в сб.: Advances in heterocyclic chemistry, ed. by A.R.
Katritzky and A. I. Boulton, v. 19, N. Y. S. F.-L., 1976, p. 123-214. В.П.Литвинов.


