ФРИСА ПЕРЕГРУППИРОВКА,
превращение сложных эфиров фенолов в орто- или пара-ацилфенолы
под действием к-т Льюиса, напр.:
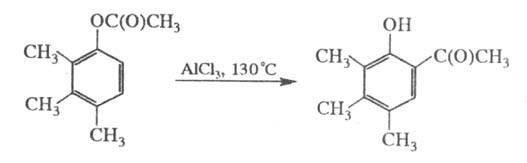
Ф. п. проводят в орг. р-рителе
(обычно в PhNO2, PhCl, CS2, Cl2CHCHCl2)
или в его отсутствие (обычно, когда требуется нагревание св. 70 0C).
В качестве к-ты Льюиса
обычно используют AlCl3 (в стехиометрич. или неск. большем кол-ве),
реже - TiCl4, SnCl4, FeCl3, ZnCl2-
В нек-рых случаях хорошие результаты дает применение безводного HF.
В р-цию вступают эфиры
одно- и многоатомных фенолов алифатич. и ароматич. карбоновых к-т. В качестве
заместителей в ароматич. ядре могут присутствовать AIk, OAIk, RC(O), Hal и др.
Присутствие мета-ориентирующего заместителя обычно препятствует Ф. п.
Алкильные группы в орто-положении и пара(мета)-положении способствуют
миграции ацильной группы в основном соотв. в пара- и орто-положение.
Нередко в жестких условиях наблюдается миграция алкильных заместителей, что
обусловлено катали-тич. действием к-ты Льюиса.
Низкие т-ры (25-60 0C)
способствуют образованию па-ра-ацилфенолов, более высокие - орто-производных
(напр., при 25 0C из м-крезилацегата образуется 80% пара-ацильного
производного, а при 165 0C - 95% орто-замещенного продукта).
Выходы конечных продуктов и соотношение образующихся изомеров колеблются в очень
широких пределах и зависят как от строения сложного эфира, так и условий проведения
р-ции.
Механизм Ф. п. до конца
не выяснен. Предполагают, что перегруппировка идет целиком по межмол. или внутри-мол.
механизму, либо частично по тому и др. пути. Как и в Фриделя - Крафтса реакции
вначале между субстратом и к-той Льюиса образуется комплекс типа R(ArO)C
=
=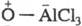
Ф.п. можно осуществлять
также при действии УФ облучения в отсутствие катализатора (т.наз. фотоперегруппировка
Фриса). В этом случае р-ция идет по радикальному механизму (вначале образуется
радикальная пара [ArO· ·COR], стабилизированная клеткой р-рителя).
При действии трифторметансульфокислоты
на арилбензо-аты Ф. п. протекает обратимо (достигается равновесие). При нагр.
пара-ацилфенолов (конечных продуктов Ф. п.) с H2SO4 или
H3PO4 образуются с хорошим выходом соответствующие сложные
эфиры фенолов (т. наз. обратная р-ция Фриса).
В р-цию, подобную Ф. п.,
вступают эфиры сульфокислот, напр.:
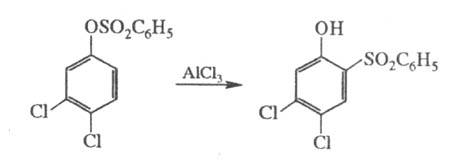
Ф. п. широко используют
в синтезе фенолкетонов. Она имеет определенные преимущества перед р-цией Фриделя
-Крафтса, в частности, зачастую обеспечивает более высокие выходы конечных продуктов.
Перегруппировка открыта К. Фрисом и Ж. Финком в 1908.
Лит.: Бласт А.,
в сб.: Органические реакции, пер. с англ., в. 1, M., 1948; Mарч Дж., Органическая
химия, пер. с англ., т. 2, M., 1987, с. 374-75.
Г.И. Дрозд.


