ХЛОРАЛЬ (трихлорацетальдегид, трихлоруксусный
альдегид) СС13СНО, мол. м. 147,4; бесцв. жидкость с резким запахом;
т. пл. -57,5 °С, т. кип. 97,75 °С;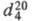 1,5121;
1,5121;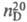 1,4557; давление пара (кПа) 0,13 (-30 °С), 4,25 (20 °С), 108 (100 °С);
1,4557; давление пара (кПа) 0,13 (-30 °С), 4,25 (20 °С), 108 (100 °С);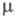 5,27 x 10-30 Кл x м;
5,27 x 10-30 Кл x м;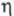 (мПа x с) 1,077 (22,5 °С), 0,533 (80 °С);
(мПа x с) 1,077 (22,5 °С), 0,533 (80 °С);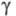 26,2 мН/м (50 °С);
26,2 мН/м (50 °С);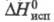 240,6 кДж/кг;
240,6 кДж/кг;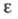 7,580
(-40,1 °С), 4,228 (62,1 °С); раств. в орг. р-рителях; в воде не раств.,
но реагирует с ней с образованием водорастворимого хлораль-гидрата СС13СН(ОН)2,
мол. м. 165,2; т. пл. 51,4 °С, т.кип. 97,5 С,
7,580
(-40,1 °С), 4,228 (62,1 °С); раств. в орг. р-рителях; в воде не раств.,
но реагирует с ней с образованием водорастворимого хлораль-гидрата СС13СН(ОН)2,
мол. м. 165,2; т. пл. 51,4 °С, т.кип. 97,5 С,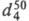 1,619; последний раств. в этаноле, диэтиловом эфире, слабо раств. в бензоле,
сероуглероде.
1,619; последний раств. в этаноле, диэтиловом эфире, слабо раств. в бензоле,
сероуглероде.
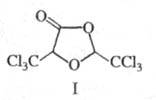
X. вступает в р-ции с др. нуклеофилами, давая твердые хорошо кристаллизующиеся устойчивые аддукты, напр. с NH3 - хлоральаммиак CC13CH(OH)NH2, с алкоголятами -хлоральалкоголяты CC13CH(OH)OR (полуацетали) или ацетали CC13CH(OR)2. При кипячении водных р-ров X. образуется глиоксиловая к-та НС(О)СООН; при действии щелочей -СНС13 и соль муравьиной к-ты; при нагр. с H2SO4 - хлоралид (ф-ла I; т. пл. 116 °С). Конц. HNO3 окисляет X. до СС13СООН (с выделением NO и NO2); при действии восстановителей, напр, изопропилата алюминия, образуется трихлорэтанол:
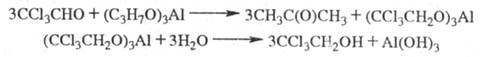
Хлорирование X. при т-рах выше 100 °С или
УФ освещении приводит к образованию СС14, СО и НС1.
При хранении X. медленно полимеризуется
в белую аморфную массу (метахлораль, парахлораль), не раств. в воде, разбавленных
к-тах, большинстве орг. р-рителей. Скорость полимеризации резко возрастает
в присут. H2SO4, (CH3)3N, А1С13
и др. катализаторов. При пиролизе (160-180 °С) полимер деполимеризуется
с образованием мономерного X.
В пром-сти X. получают хлорированием этанола
в каскаде двух реакторов: в первый реактор вводится хлор, частично прохлорированный
спирт и вода, необходимая для гидролиза промежут. продуктов хлорирования,
т-ра в реакторе (до 90 °С) поддерживается за счет теплоты р-ции. Во втором
реакторе реагирует непрореагировавший в первом хлор и свежий этанол. Техн.
продукт содержит 80-85% хлоральгидрата, 10-15% хлоральалкоголята, примеси
НС1 и дихлорацетальдегида. X. выделяют обработкой смеси конц. H2SO4
с послед. разделением слоев, перегонкой и ректификацией.
X. может быть получен также хлорированием
этиленхлоргидрина, ацетальдегида или смеси диэтилового эфира с водой при
25-90 °С, а также из СС14 и СН2О при пропускании
их паров над тонко раздробленными металлами (Сu) при 300 °С.
Используют X. в осн. для произ-ва инсектицидов
и гербицидов, в небольших кол-вах для получения фармацевтич. препаратов.
В виде хлоральгидрата ограниченно применялся как успокаивающее, снотворное
и анестезирующее средство.
X.- трудногорючая жидкость. ПДК в воде
водоемов хозяйств.-бытового пользования 0,2 мг/л.
Лит.: Промышленные хлорорганические продукты. Справочник, под ред. Л. А. Ошина, М., 1978, с. 159-67.
Ю. А. Трегер.


