ЦЕЗИЯ ОКСИД Cs2O, кристаллы
(табл.), расплывающиеся на воздухе; в вакууме (10-3 Па) возгоняется
при 350-450 °С, при 500 °С разлагается: 2Cs2O Cs2O2
+ 2Cs; энергично реагирует с водой, давая CsOH, с влажным СО2,
при 150-200 °С - с Н2, F2, C12, а также
с расплавл. S; разлагается на свету; получают медленным окислением Cs кислородом
(2/3 стехиометрич. кол-ва), остаток Cs отгоняют в вакууме при 180-200 °С.
При окислении Cs кислородом получают также его пероксид и надпероксид.
Cs2O2
+ 2Cs; энергично реагирует с водой, давая CsOH, с влажным СО2,
при 150-200 °С - с Н2, F2, C12, а также
с расплавл. S; разлагается на свету; получают медленным окислением Cs кислородом
(2/3 стехиометрич. кол-ва), остаток Cs отгоняют в вакууме при 180-200 °С.
При окислении Cs кислородом получают также его пероксид и надпероксид.
СВОЙСТВА ОКСИДА, ПЕРОКСИДА И НАДПЕРОКСНДА
ЦЕЗИЯ
|
Показатель
|
Cs2O
|
Cs2O2
|
CsO2
|
|
|
Цвет
|
Коричнево-красный
|
Бледно-желтый
|
Золотисто -коричневый
|
|
|
Сингония
|
Гексагон.
|
Ромбич.
|
Тетрагон.
|
|
|
Параметры кристаллич.
решетки, нм: а
|
0,674 |
0,4322 |
0,4477 |
|
|
b
|
—
|
0,7517
|
—
|
|
|
с
|
1,882
|
0,6340
|
0,7350
|
|
|
Пространств.
группа
|
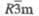 |
Immm
|
14/ттт
|
|
|
Т. пл., °С
|
595
|
594
|
130*
|
|
|
Плотн., г/см3
|
4,36
|
4,47 (15 °С)
|
3,76 (19 °С)
|
|
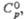 Дж/(моль x К)
Дж/(моль x К) |
76,0
|
95,0
|
79,1
|
|
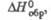 кДж/моль
кДж/моль |
-346,4
|
-440
|
-286
|
|
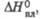 кДж/моль
кДж/моль |
20
|
22
|
—
|
|
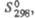 Дж/(моль x К)
Дж/(моль x К) |
146,9
|
180
|
142
|
|
*Т-ра полиморфного перехода, ниже -263,6 "Сив интервале от -263,6 до -83 oС существуют две ромбич. модификации.
Пероксид Cs2O2 -
гигроскопичные кристаллы, выше 650 °С разлагается с выделением атомарного
кислорода и активно окисляет Ni, Ag, Pt, Au; давление диссоциации 2261
Па (1103 °С); раств. в ледяной воде без разложения, выше 25 °С гидролизуется:
2Cs2O2 + 2Н2О 4CsOH + О2;
4CsOH + О2;
в к-тах раств. с образованием Н2О2;
получают окислением Cs или его р-ра в жидком NH3 дозированным
кол-вом О2.
Надпероксид CsO2 выше 350 °С
диссоциирует с выделением О2, давление диссоциации 931 Па (400
С), 6783 Па (973 °С); очень сильный окислитель, окисляет, напр., ReO2
до
Cs3ReO5, МnО2 - до Cs2MnO4,
SeO2 - до Cs2SeO4; реагирует с Н2О,
СО2, H2 с выделением О2; чистый CsO2
получают сжиганием металла в избытке О2, др. способы - окисление
кислородом р-ра Cs в жидком NH4, амальгамы Cs, расплавов CsOH
и Cs2O.
Ц. о.- компонент сложных фотокатодов,
спец. стекол и катализаторов; Cs2O2, CsO2
- источники О2 и его регенераторы в космич. и подводных кораблях.
Л. И. Покровская.


