ЭЛЕКТРОПРОВОДНОСТЬ ЭЛЕКТРОЛИТОВ,
способность
электролитов проводить электрич. ток при приложении электрич. напряжения.
Носителями тока являются положительно и отрицательно заряженные ионы -
катионы и анионы, к-рые существуют в р-ре вследствие электролитич. диссоциации.
Ионная Э. э., в отличие от электронной, характерной для металлов, сопровождается
переносом в-ва к электродам с образованием вблизи них новых хим. соед.
(см. Электролиз). Общая (суммарная) проводимость состоит из проводимости
катионов и анионов, к-рые под действием внешнего электрич. поля движутся
в противоположных направлениях. Доля общего кол-ва электричества, переносимого
отд. ионами, наз. числами переноса, суммак-рых для всех видов ионов, участвующих
в переносе, равна единице.
Количественно Э. э. характеризуют эквивалентной
электропроводностью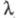 - проводящей способностью всех ионов, образующихся в 1 грамм-эквиваленте
электролита. Величина
- проводящей способностью всех ионов, образующихся в 1 грамм-эквиваленте
электролита. Величина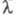 связана с уд. электропроводностью
связана с уд. электропроводностью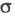 соотношением:
соотношением:
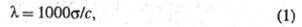
где с - концентрация р-ра в г-экв/л.
Эквивалентная электропроводность зависит от природы растворенного в-ва
и р-рителя, структуры р-ра, а также от концентрации, т-ры, давления. Предельно
разбавленному р-ру, в к-ром все молекулы диссоциированы на ионы, соответствует
предельное значение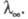 В соответствии с Кольрауша законом
В соответствии с Кольрауша законом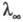 равна
сумме эквивалентных электропроводностей катионов и анионов. Эквивалентная
электропроводность отд. иона пропорциональна скорости его движения в р-ре
и характеризует подвижность иона в р-ре.
равна
сумме эквивалентных электропроводностей катионов и анионов. Эквивалентная
электропроводность отд. иона пропорциональна скорости его движения в р-ре
и характеризует подвижность иона в р-ре.
Описание концентрац. зависимости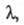 как
и других св-в р-ров электролитов (см. Растворы электролитов), обычно
базируется на ионном подходе, в рамках к-рого р-ритель рассматривается
как бесструктурная диэлектрич. среда, в к-рой ионы движутся в соответствии
с законами гидродинамики и характером межионного взаимодействия. Простейшей
моделью является модель заряженных твердых сфер, движущихся в вязком р-рителе
под влиянием силы, обусловленной градиентом потенциала. При этом сила сопротивления
движению иона в р-ре определяется ур-нием Стокса (см. Вискозиметрия).
В
рамках применимости этого ур-ния выполняется правило Вальдена-Писаржевского,
в соответствии с к-рым для одного и того же электролита в любых р-рителях
произведение предельного значения эквивалентной электропроводности
как
и других св-в р-ров электролитов (см. Растворы электролитов), обычно
базируется на ионном подходе, в рамках к-рого р-ритель рассматривается
как бесструктурная диэлектрич. среда, в к-рой ионы движутся в соответствии
с законами гидродинамики и характером межионного взаимодействия. Простейшей
моделью является модель заряженных твердых сфер, движущихся в вязком р-рителе
под влиянием силы, обусловленной градиентом потенциала. При этом сила сопротивления
движению иона в р-ре определяется ур-нием Стокса (см. Вискозиметрия).
В
рамках применимости этого ур-ния выполняется правило Вальдена-Писаржевского,
в соответствии с к-рым для одного и того же электролита в любых р-рителях
произведение предельного значения эквивалентной электропроводности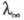 на вязкость р-рителя
на вязкость р-рителя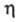 является постоянной величиной, к-рая не зависит от природы р-рителя, но
является ф-цией т-ры. Сравнительно хорошо это правило выполняется только
для слабо сольватир. ионов, в частности ионов, имеющих большие размеры
в кристаллич. фазе. С увеличением концентрации значение
является постоянной величиной, к-рая не зависит от природы р-рителя, но
является ф-цией т-ры. Сравнительно хорошо это правило выполняется только
для слабо сольватир. ионов, в частности ионов, имеющих большие размеры
в кристаллич. фазе. С увеличением концентрации значение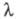 уменьшается в осн. в р-рах слабых электролитов и в области малых концентраций
удовлетворительно описывается законом разведения Оствальда (см. Электролитическая
диссоциация).
уменьшается в осн. в р-рах слабых электролитов и в области малых концентраций
удовлетворительно описывается законом разведения Оствальда (см. Электролитическая
диссоциация).
В р-рах сильных электролитов концентрац.
зависимость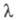 определяется межионным взаимодействием. В области применимости Дебая-Хюккеля
теории имеются две причины для торможения ионов вследствие межионного
взаимодействия. Первая из них связана с тем, что движение иона тормозится
ионной атмосферой, к-рая имеет заряд, противоположный центральному иону,
и под влиянием поля движется в направлении, противоположном перемещению
иона (электрофоретич. эффект). Вторая причина связана с тем, что при движении
иона под действием электрич. поля его ионная атмосфера деформируется и
теряет сферич. симметрию, причем большая часть заряда ионной атмосферы
концентрируется позади центрального иона (релаксац. эффект). Учет обоих
эффектов приводит кур-нию Онсагера:
определяется межионным взаимодействием. В области применимости Дебая-Хюккеля
теории имеются две причины для торможения ионов вследствие межионного
взаимодействия. Первая из них связана с тем, что движение иона тормозится
ионной атмосферой, к-рая имеет заряд, противоположный центральному иону,
и под влиянием поля движется в направлении, противоположном перемещению
иона (электрофоретич. эффект). Вторая причина связана с тем, что при движении
иона под действием электрич. поля его ионная атмосфера деформируется и
теряет сферич. симметрию, причем большая часть заряда ионной атмосферы
концентрируется позади центрального иона (релаксац. эффект). Учет обоих
эффектов приводит кур-нию Онсагера:
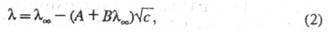
где А и В - эмпирич. постоянные,
являющиеся ф-циями т-ры, вязкости и диэлектрич. проницаемости р-рителя.
Как и теория Дебая-Хюккеля, ур-ние Онсагера
ограничено областью умеренно разбавленных р-ров. Для описания концентрир.
р-ров возникает необходимость в учете некулоновской части межионного взаимод.,
в частности в учете ионных размеров. Для этой цели применяют методы кинетич.
теории ионных систем. К дополнит. уменьшению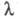 приводит образование ионных ассоциатов - пар, тройников и т. п., к-рое,
как и эффект неполной диссоциации, сокращает общее число своб. ионов в
р-ре. Для учета этого эффекта в ур-нии Онсагера заменяют общую концентрацию
ионов концентрацией своб. ионов
приводит образование ионных ассоциатов - пар, тройников и т. п., к-рое,
как и эффект неполной диссоциации, сокращает общее число своб. ионов в
р-ре. Для учета этого эффекта в ур-нии Онсагера заменяют общую концентрацию
ионов концентрацией своб. ионов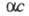 (
(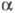 - степень
электролитич. диссоциации), что приводит к ур-нию Фуосса-Онсагера:
- степень
электролитич. диссоциации), что приводит к ур-нию Фуосса-Онсагера:
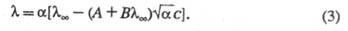
В переменных электрич. полях при достаточно
высокой частоте ион не уходит далеко от центра ионной атмосферы, вследствие
чего она не деформируется. Обусловленный деформацией релаксац. эффект не
возникает, что приводит к увеличению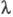 -т.наз.
эффект Дебая-Фалькенхагена. Величина
-т.наз.
эффект Дебая-Фалькенхагена. Величина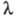 возрастает также в постоянных электрич. полях достаточно высокой напряженности
(104-105 В/см). В этих условиях ионы движутся настолько
быстро, что ионная атмосфера не успевает образоваться, вследствие чего
практически отсутствуют и релаксац. и электрофоретич. эффекты. В результате
возрастает также в постоянных электрич. полях достаточно высокой напряженности
(104-105 В/см). В этих условиях ионы движутся настолько
быстро, что ионная атмосфера не успевает образоваться, вследствие чего
практически отсутствуют и релаксац. и электрофоретич. эффекты. В результате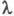 стремится к предельному значению
стремится к предельному значению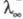 (т. наз. эффект Вина). В слабых электролитах эффект Вина вызывается также
смещением диссоциативного равновесия в сильном электрич. поле в сторону
образования ионов.
(т. наз. эффект Вина). В слабых электролитах эффект Вина вызывается также
смещением диссоциативного равновесия в сильном электрич. поле в сторону
образования ионов.
Влияние т-ры и давления на Э. э. обусловлено
изменением предельного значения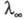 вследствие изменения структуры р-рителя и характера ион-молекулярного взаимод.,
изменения влияния межионного взаимод. и смещения диссоциативного равновесия.
Более детальное описание механизма Э. э. в широкой области концентраций,
т-р и давлений возможно в рамках ион-молекулярного подхода. При этом уд.
электропроводность рассчитывают через электрич. поток j(t)=
вследствие изменения структуры р-рителя и характера ион-молекулярного взаимод.,
изменения влияния межионного взаимод. и смещения диссоциативного равновесия.
Более детальное описание механизма Э. э. в широкой области концентраций,
т-р и давлений возможно в рамках ион-молекулярного подхода. При этом уд.
электропроводность рассчитывают через электрич. поток j(t)=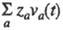 и автокорреляц. ф-цию
и автокорреляц. ф-цию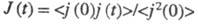 с помощью соотношения:
с помощью соотношения:

где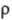 -
кол-во ионов электролита в единице объема р-ра, е -элементарный
электрич. заряд,
-
кол-во ионов электролита в единице объема р-ра, е -элементарный
электрич. заряд,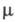 - приведенная масса катиона и аниона, za - степень окисления
иона сорта a, vа(t) - его скорость в момент времени
t.
- приведенная масса катиона и аниона, za - степень окисления
иона сорта a, vа(t) - его скорость в момент времени
t.
Специфич. механизм электропроводности
характерен для к-т и оснований, содержащих соотв. ионы Н+ и
ОН-, к-рые в водных р-рах (или других протонных р-рителях) имеют
подвижность на порядок больше остальных ионов. Для объяснения аномально
высокой проводимости ионов Н+ и ОН-предполагается,
что под влиянием электрич. поля протоны перемещаются не только путем миграции,
но и по механизму протонного обмена, включающему перенос протона в кислой
среде от ионов гидроксония Н3О+ к молекуле воды,
а в щелочной - от молекулы воды к иону ОН-.
Эксперим. изучение Э. э.- важное направление
физико-химического
анализа, поскольку зависимость Э. э. от состава р-ра позволяет судить
о концентрации солей, качественный, состав к-рых известен (см. также Кондуктометрия).
Измерения
l
используют для определения подвижностей ионов.
Лит.: Скорчеллетти В. В., Теоретическая электрохимия, 4 изд., Л., 1974; Измайлов Н. А., Электрохимия растворов, 3 изд., М., 1976; Эрдеи-Груз Т., Явления переноса в водных растворах, пер. с англ., М., 1976. См. также лит. к ст. Растворы электролитов.
М. Ф. Головко.


