ЭЛЕКТРОЦИКЛИЧЕСКИЕ РЕАКЦИИ,
внутримол.
перициклические
реакции, при к-рых образуется новая
s-связь
между концами линейных молекул или их отдельных линейных участков, представляющих
собой сопряженные системы; при этом число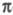 -связей
уменьшается на единицу:
-связей
уменьшается на единицу:

К Э. р. относят также обратный процесс
раскрытия цикла с разрывом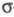 -связи
и образованием сопряженной системы, напр.:
-связи
и образованием сопряженной системы, напр.:
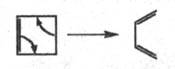
Существует два стереохимически разл. пути
Э. р.- конротаторный и дисротаторный (см. Вудворда-Хофмана правила).
Простейшая Э. р.- раскрытие циклопропанового
кольца с образованием аллильного катиона (2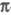 -электронная
система), осуществляющееся в условиях сольволиза дисротаторным путем:
-электронная
система), осуществляющееся в условиях сольволиза дисротаторным путем:
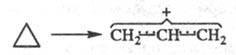
Если трехчленный цикл входит в бициклич.
систему, то его раскрытие зависит от размера второго цикла и положения
уходящей группы относительно плоскости трехчленного цикла. Для эндо-производных
сольволиз протекает быстрее, чем для экзо-изомеров (в случае моноциклич.
циклопропанов этот эффект выражен слабее).
Подробно изучена Э. р. превращения циклобутена
в 1,3-бутадиен (4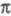 -электронная
система), проходящая в условиях термолиза по конротаторному механизму.
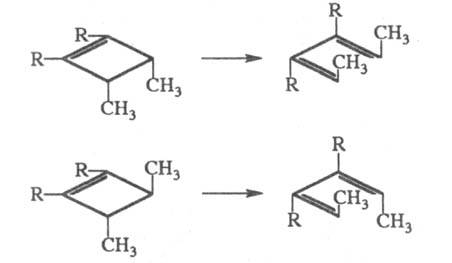
Р-ция высокостереоспецифична: из цис-3,4-диметилциклобутенов получают
только цис, транс-диены, а из транс-изомеров - только транс,
транс-диены:
-электронная
система), проходящая в условиях термолиза по конротаторному механизму.
Р-ция высокостереоспецифична: из цис-3,4-диметилциклобутенов получают
только цис, транс-диены, а из транс-изомеров - только транс,
транс-диены:
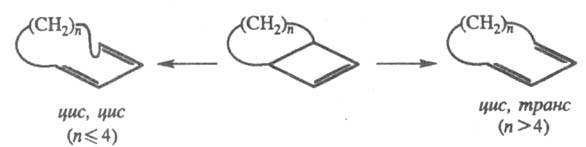
В случае бициклобугенов, в соответствии
с правилами Вудворда-Хофмана, конротаторное раскрытие колец должно приводить
к стерически напряженным цис, транс-циклодиенам, содержащим транс-сочлененную
двойную связь. Поэтому для бициклоалкенов при п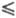 4
предпочтителен запрещенный механизм раскрытия, приводящий к цис, цис-циклодиенам.
4
предпочтителен запрещенный механизм раскрытия, приводящий к цис, цис-циклодиенам.
Фотохим. взаимопревращения бутадиенов и
циклобутенов протекают по дисротаторному механизму.
В Э. р. участвуют другие 4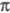 -электронные
системы, напр. трехчленные циклы, содержащие гетероатом с неподеленной
электронной парой; раскрытие кольца для этих систем протекает в термич.
условиях по конротаторному механизму.
-электронные
системы, напр. трехчленные циклы, содержащие гетероатом с неподеленной
электронной парой; раскрытие кольца для этих систем протекает в термич.
условиях по конротаторному механизму.
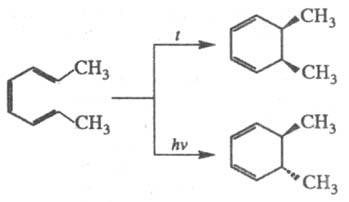
Термич. дисротаторная циклизация
транс,
цис, транс-2,4,6-октатриена (6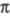 -электронная
система) приводит почти исключительно к цис-5,6-диметил-1,3-циклогексадиену;
фотохим. циклизация протекает конротаторно с образованием транс-изомера:
-электронная
система) приводит почти исключительно к цис-5,6-диметил-1,3-циклогексадиену;
фотохим. циклизация протекает конротаторно с образованием транс-изомера:
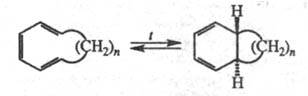
Циклич. триеновые системы в условиях термич. Э. р. находятся в равновесии с бициклич. продуктом, при этом чем более напряжена структура бициклич. соед. (т. е., чем меньше п), тем в большей степени равновесие сдвинуто в сторону моноциклич. структуры:
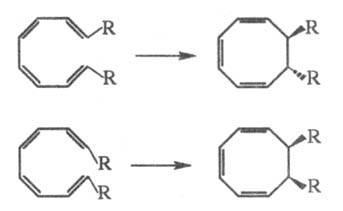
Э. р. с участием 8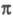 -электронных
систем протекают при нагр. по конротаторному механизму, напр.:
-электронных
систем протекают при нагр. по конротаторному механизму, напр.:
Термин Э. р. введен Р. Вудвордом и Р. Хофманом в 1969.
Лит.: Вудворд Р., Хоффман Р., Сохранение орбитальной симметрии, пер. с англ., М., 1971; Джилкрист Т., Сторр Р., Органические реакции и орбитальная симметрия, пер. с англ., М., 1976; Пирсон Р., Правила симметрии в химических реакциях, пер. с англ., М., 1979.
М. Е. Клецкий.


