ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ (теплота образования), энтальпия р-ции образования данного в-ва (или р-ра) из заданных исходных в-в. Э. о. хим. соединения наз. энтальпию р-ции образования данного соед. из простых в-в. В качестве простых в-в выбирают хим. элементы в их естественном фазовом и хим. состоянии при данной т-ре. Так, при 298 К для хлора простым в-вом служит газообразный хлор, состоящий из молекул С12, а для калия - металлич. К. Энтальпия образования твердого КС1 при 298 К - это энтальпия р-ции:
К(тв.) + 1/2С12= КС1(тв.).
Э. о. КС1 (тв.) при 500 К соответствует
р-ции: К(жидкий) + 1/2C12 = КС1(тв.),
т. к. естественным фазовым состоянием (простым в-вом) для калия становится
уже не кристалл, а жидкость (т-ра плавления К 336,66 К).
Э. о. может быть определена при любой
т-ре. Стандартные Э. о.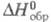 соответствуют р-циям образования, при к-рых и простые в-ва, и получающееся
соед. находятся при давлении 1 атм (1,01 x 105 Па). По определению,
для всех простых в-в при любой т-ре
соответствуют р-циям образования, при к-рых и простые в-ва, и получающееся
соед. находятся при давлении 1 атм (1,01 x 105 Па). По определению,
для всех простых в-в при любой т-ре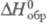 =
0 (см. Стандартное состояние). Для большинства хим. соед. Э. о.-
отрицат. величины.
=
0 (см. Стандартное состояние). Для большинства хим. соед. Э. о.-
отрицат. величины.
Единицы измерения Э. о.- Дж/г, Дж/моль.
В термодинамике р-ров (расплавов) под
Э. о. понимают изменение энтальпии при изотермо-изобарном образовании 1
моля (1 г) р-ра (расплава) данного состава из чистых компонентов. Так,
в двухкомпонентной системе KF-A1F3 Э. о. расплава 50 %-ного
молярного состава соответствует процессу: 1/2КF(жидкий)
+ 1/2А1F3(жидкий) = КF-А1F3(расплав,
50 мол. %).
Определение стандартных Э. о. смесей возможно
при любой т-ре, как и Э. о. хим. соединений. Э. о. смеси данного состава
наз. часто энтальпией смешения. Неидеальные р-ры характеризуются избыточной
Э. о., к-рая представляет собой разницу между реальной Э. о. фазы данного
состава и Э. о. гипотетич. идеального р-ра того же состава (см. Растворы
неэлектролитов).
Э. о. определяют экспериментально калориметрич.
измерениями. Второе и третье начала термодинамики позволяют получать Э.
о. из эксперим. данных. Теоретич. расчеты Э. о. хим. соед. пока неосуществимы.
Возможны эмпирич. оценки Э. о., напр., из Э. о. родственных соединений.
Э. о. хим. соединений табулированы в термодинамич.
справочниках и банках информации.
М. В. Коробов.


