
Эфирная группировка планарна или близка
к планарной: простая связь С — О (структура I) имеет конформацию с цисоидным
расположением карбонильной двойной связи и связи О — R. Длина связи С =
О в разл. Э. с. 0,119-0,122 нм, связи С — О 0,131-0,136 нм, углы ОСО 122-126°,
СОС 113-118°.
По номенклатуре ИЮПАК названия Э. с. производят
от назв. апкильной или арильной группы гидроксильного компонента и названия
к-ты путем замены окончания "овая" на суффикс "ат", напр.: C2H5COOC2H5
- этилпропионат, CH3OSO2OH - метилсульфат. Нек-рые
Э. с. имеют тривиальные названия.
Э. с.- главная составная часть жиров,
восков, спермацета; входят в состав мн. эфирных масел.
Физические свойства. Э. с. низших
карбоновых к-т и простейших спиртов - бесцв. летучие жидкости, часто с
приятным фруктовым запахом; Э. с. высших карбоновых к-т - твердые бесцв.
в-ва, почти лишенные запаха. Низшие Э. с. минер. к-т (алкилсульфиты, алкилсульфаты,
алкилбораты) - маслянистые жидкости с приятным запахом; алкилсульфаты,
начиная с С9Н17,- твердые соед. Т-ры кипения Э. с.
низших спиртов ниже, чем соответствующих к-т; т-ры кипения сульфитов обычно
ниже, чем сульфатов. Э. с. плохо раств. в воде, хорошо - в орг. р-рителях,
обладают значит. дипольным моментом (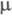 5,67 х 10-30-6,66 х 10-30 Кл х м).
5,67 х 10-30-6,66 х 10-30 Кл х м).
В ИК спектрах Э. с. присутствуют характеристич.
полосы в области 1750-1700 см-1 (валентные колебания группы
С = О) и 1275-1050 см-1 (валентные колебания группы С — О).
В УФ спектрах наблюдаются слабые полосы при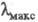 195-210 нм
195-210 нм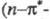 переход); для
переход); для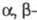 ненасыщ.
эфиров сильные полосы при
ненасыщ.
эфиров сильные полосы при 210 нм
210 нм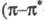 -переход),
по мере увеличения ненасыщенности полоса сдвигается в длинноволновую область.
В спектрах ПМР хим. сдвиг
-переход),
по мере увеличения ненасыщенности полоса сдвигается в длинноволновую область.
В спектрах ПМР хим. сдвиг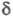 3,7-4,1 м. д. (
3,7-4,1 м. д. (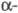 Н-атом
спиртового остатка) и
Н-атом
спиртового остатка) и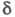 2-2,2 м. д. (
2-2,2 м. д. (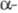 Н-атом
кислотного остатка).
Н-атом
кислотного остатка).
Химические свойства. Большинство р-ций Э. с. связано с нуклеоф. атакой по карбонильному атому углерода и замещением алкоксигруппы:
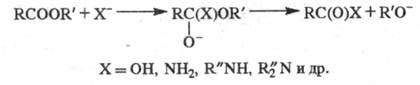
Гидролиз Э. с. протекает как в кислой (минер.
к-ты), так и в щелочной среде [водные или спиртовые р-ры NaOH, КОН, а также
Ва(ОН)2, Са(ОН)2]:
Кислотный гидролиз - обратимый процесс,
щелочной -практически необратим, т. к. карбоксилат-анион RCOO-
не м. б. атакован нуклеофилом. Скорость гидролиза увеличивается с повышением
т-ры и с увеличением мол. массы эфира. Многие Э. с. (гл. обр. жиры) гидролизуются
под действием ферментов.
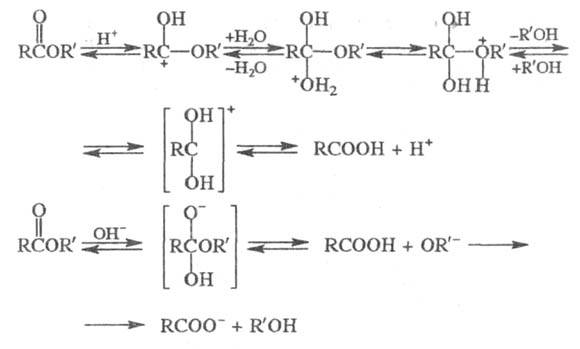
При взаимод. Э. с. со спиртами происходит
переэтерификация (см. ниже); кат.- H2SO4 или сухой
НС1 либо алкоголят-ион. Аммонолиз и аминолиз Э. с. приводит соотв. к амидам
RCONH2 и N-замещенным амидам RCONR'R"; катализаторами служат
чаще всего NH4C1 или СН3ОК, р-рителями - диэтиловый
эфир, бензол или сам амин (для ароматич. аминов). Низкомол. Э. с. реагируют
с NH3 при комнатной т-ре, высокомол.- при повышенных т-ре и
давлении. Иногда аммонолиз проводят при низкой т-ре, чтобы избежать побочных
р-ций, напр.:
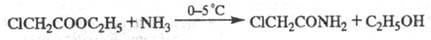
Особенно легко протекает внутримол. аминолиз;
напр.,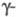 аминоэфиры
циклизуются уже при комнатной т-ре, давая пирролидоны:
аминоэфиры
циклизуются уже при комнатной т-ре, давая пирролидоны:

При взаимод. Э. с. с NH2OH образуются
гидроксамовые к-ты RCONHOH, с гидразином - гидразиды RCONHNH2,
с ацеталями или карбоновыми к-тами в присут. минер, к-т происходит обменная
р-ция (см. Ацидолиз).
Р-ции Э. с. с реактивами Гриньяра и др.
металлоорг. соед. приводят к образованию третичных спиртов (за исключением
фэрмиатов, к-рые дают вторичные спирты):
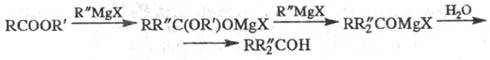
Э. с. вступают в сложноэфирную конденсацию
с соед., содержащими активную метиленовую группу (см. Клайзена конденсация),
диэфиры двухосновных к-т претерпевают внутримол. конденсацию (см. Дикмана
реакция).
Э. с., образующие стабильные карбанионы
и не проявляющие тенденции к самоконденсации, легко алкилируются; нек-рые
из таких эфиров вступают в р-ции с разрывом связи алкил-кислород, напр.:
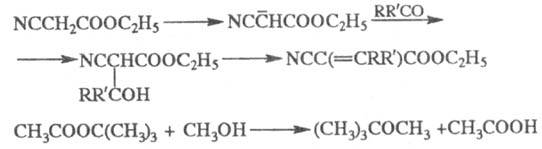
Э. с. минер. и фторзамещенных карбоновых к-т алкилируют разл. соед. в щелочной среде, напр.:
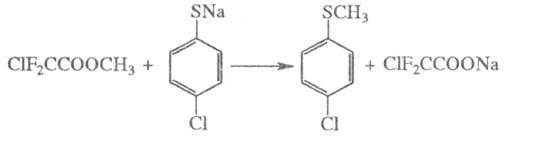
При т-ре выше 300 °С Э. с. разлагаются с образованием алкенов, пиролиз ацетатов проводят в газовой фазе при 500-600 °С:
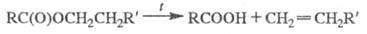
Пиролиз Э. с. жирных к-т в присут. нек-рых металлов (Mg, Zn) или их оксидов приводит к кетонам:
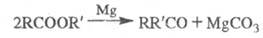
Бензоаты и оксалаты разлагаются при более
низких т-рах в жидкой фазе.
Э. с. устойчивы к действию окислителей.
Восстановление Э. с. (Na в этаноле, LiAlH4, A1H3
и др.) приводит к альдегидам, но обычно восстановление идет дальше - до
первичного спирта: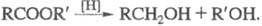 Каталитич. гидрирование Э. с. в присут. хромата (III) меди при т-ре 200-300
°С и давлении 10-30 МПа - пром. способ получения спиртов. При восстановлении
эфиров алифатич. моно- и дикарбоновых к-т Na в кипящем ксилоле образуются
ацилоины (см. Ацилоиновая конденсация).
Каталитич. гидрирование Э. с. в присут. хромата (III) меди при т-ре 200-300
°С и давлении 10-30 МПа - пром. способ получения спиртов. При восстановлении
эфиров алифатич. моно- и дикарбоновых к-т Na в кипящем ксилоле образуются
ацилоины (см. Ацилоиновая конденсация).
Получение. Наиб. широко применяют
этерификацию - взаимод. спиртов с к-тами: RCOOH + R'OH RCOOR'
+ H2O. Это - обратимая р-ция, в к-рой положение равновесия зависит
от природы и кол-ва к-ты и спирта и характеризуется равновесной концентрацией
продуктов этерификации (т. наз. предел этерификации), напр. при эквимол.
соотношении СН3СООН и C2H5OH равновесие
устанавливается, когда ~2/3 к-ты и спирта превращается
в эфир. На скорость достижения предела этерификации влияют т-ра и катализаторы
(сильные к-ты и их ангидриды, арилсульфоновые к-ты, кислые соли и кислые
катионообменные смолы). Для повышения выхода воду из реакц. среды удаляют
азеотропной дистилляцией. Легче всего этерифицируются первичные спирты,
наиб. трудно - третичные.
RCOOR'
+ H2O. Это - обратимая р-ция, в к-рой положение равновесия зависит
от природы и кол-ва к-ты и спирта и характеризуется равновесной концентрацией
продуктов этерификации (т. наз. предел этерификации), напр. при эквимол.
соотношении СН3СООН и C2H5OH равновесие
устанавливается, когда ~2/3 к-ты и спирта превращается
в эфир. На скорость достижения предела этерификации влияют т-ра и катализаторы
(сильные к-ты и их ангидриды, арилсульфоновые к-ты, кислые соли и кислые
катионообменные смолы). Для повышения выхода воду из реакц. среды удаляют
азеотропной дистилляцией. Легче всего этерифицируются первичные спирты,
наиб. трудно - третичные.
Этерификацией наз. также методы получения
Э. с. ацилированием спиртов, алкилированием к-т диазоалканами либо солей
алкилгалогенидами.
Другой распространенный способ получения
Э. с- переэтерификация - замена одного спиртового или кислотного остатка
в молекуле Э. с. на другой. Осуществляют р-цию взаимод. Э. с. со спиртами,
карбоновыми к-тами или др. Э. с. в присут. алкоголятов, щелочей, НС1, BF3,
солей нек-рых металлов, напр.:
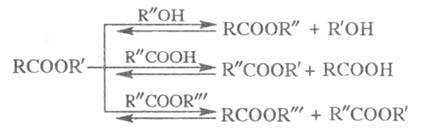
Равновесие смещают вправо путем отгонки
более летучих спирта, к-ты или эфира. Метод используют для получения Э.
с., к-рые нельзя получить этерификацией, напр. виниловые или изопропиловые
эфиры высших к-т.
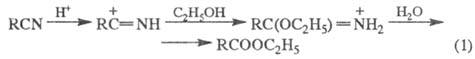
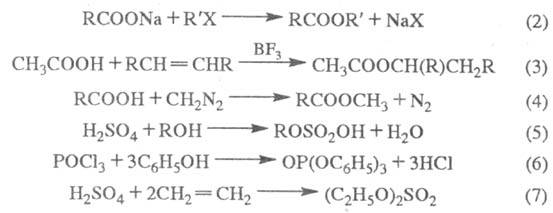
Э. с. образуются также кислотным алкоголизмом
нитрилов (кат.- H2SO4, HC1, n-толуолсульфокислота;
р-ция 1); алкилированием карбоксилат-анионов (к-т или их солей) алкилгалогенидами,
алкенами в присут. катализаторов (2,3); из альдегидов по Тищенко реакции;
метиловые
эфиры - р-цией к-т с диазометаном (4); эфиры минер. к-т - взаимод. последних,
а также их галогенангадридов со спиртами или фенолами (5,6) либо минер.
к-т с олефинами (7):
Для получения Э. с. используют окисление: кетонов Н2О2 или надкислотами (Байера-Виллигера реакция), ацетиленовых производных (8), соед., содержащих аллильную группу (9) и др.:
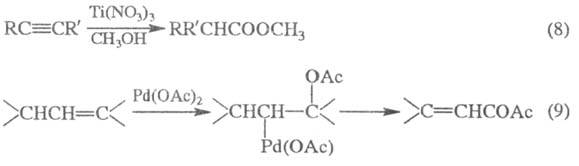
Э. с. высших дикарбоновых к-т получают из солей кислых эфиров дикарбоновых к-т в условиях электрохим. р-ции Кольбе:
2ROOC(CH2)nCOONa ROOC(CH2)2nCOOR
ROOC(CH2)2nCOOR
Э. с. серной и фосфорной к-т образуются при окислении соответствующих сульфитов и фосфитов.
Определение. Для обнаружения Э. с. используют их р-цию с гидроксиламином: образующиеся гидроксамовые к-ты дают с FеС13 характерное красное окрашивание, для определения -кислотное число и эфирное число, а также методы хроматографии.
Применение. Э. с.- р-рители, пластификаторы,
экстрагенты, лек. средства (напр., нитроглицерин), сырье для синтеза полимеров
(напр., метилметакрилат) и фармацевтич. препаратов (напр., производных
салициловой к-ты). Э. с. серной к-ты используют как алкилирующие агенты;
Э. с. фосфорной к-ты - инсектициды, флотореагенты, присадки к маслам; низшие
Э. с. карбоновых к-т применяют в парфюмерии и пищ. пром-сти.
См. также Ацетоуксусный эфир, Винилацетат,
Глицериды, Метилметакрилат, Этилацетат и др.
Лит.: Вейганд-Хильгетаг, Методы эксперимента в органической химии, пер. с нем., М., 1968; Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 288-388; Kirk-Othmer encyclopedia, 3 ed., v. 9, N. Y., 1980, p. 311-37.
Л. Н. Максимова.


