МОЛЕКУЛЯРНОСТЬ РЕАКЦИИ,
число частиц реагентов, взаимодействующих друг с другом в одной элементарной
(простой) р-ции и превращающихся в продукты. Так, для р-ций в р-рах М. р. не
учитывает число молекул р-рителя, образующих сольватную оболочку или мол. комплексы
с реагентами, т. к. эти молекулы не входят в состав продуктов р-ции. В р-циях
замещения и элиминирования орг. соед., протекающих часто в неск. стадий, М.
р. оценивается как число молекул, претерпевающих хим. превращение в лимитирующей
стадии. Соответственно числу реагирующих частиц
различают мономолекулярные реакции, бимолекулярные реакции и тримолекулярные
реакции, отличающиеся кинетич. закономерностями и механизмом. Как правило,
молекуляр-ность простой р-ции совпадает с порядком реакции, однако бывают
и несовпадения. Напр., рекомбинации атомов в газовой фазе протекают через тройные
столкновения типа 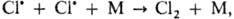 где М-третья частица. Суммарный порядок таких р-ций-третий (скорость u =
= k[М][Сl]2, где k-константа скорости), но молекуляр-ность
равна 2, т.к. в хим. взаимодействии участвуют два атома хлора, а частица М лишь
принимает на себя энергию, выделившуюся при рекомбинации атомов, не претерпевая
при этом хим. превращения.
где М-третья частица. Суммарный порядок таких р-ций-третий (скорость u =
= k[М][Сl]2, где k-константа скорости), но молекуляр-ность
равна 2, т.к. в хим. взаимодействии участвуют два атома хлора, а частица М лишь
принимает на себя энергию, выделившуюся при рекомбинации атомов, не претерпевая
при этом хим. превращения.


