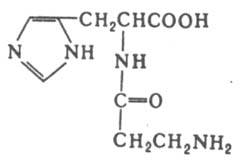
Биол. роль К. окончательно не выяснена. Установлено, что он является предшественником в биосинтезе анзерина; благоприятно влияет на гликолиз и окислит. фосфорилирование, увеличивая кол-во образующегося АТФ; повышает отношение Са/АТФ при нарушенном активном транспорте Са в пузырьках саркоплазматич. ретикулома; увеличивает эффективность активного транспорта К+ и Na+ через плазматич. мембрану; препятствует пероксидному окислению липидов; активирует восстановление поврежденных тканей. Биосинтез К. осуществляется гл. обр. в скелетных мышцах при участии малоспецифичного фермента карнозинсинтетазы по схеме:
b-Аланин + АТФ + Е D Е—b-Аланил—АМФ + ПФ;
Е—b-Аланил—АМФ + Гистидин D К. + АМФ + Е.
Е - карнозинсинтетаза, АМФ - аденозинмонофосфат, ПФ -пирофосфорная к-та. Р-ция практически необратима, т. к. ПФ быстро гидролизуется пирофосфатазой до Н3РО4. У мн. животных в корковом слое почек, печени, в обонятельной луковице, селезенке, cекрете слизистой тонкого кишечника находится фермент карнозиназа, катализирующий гидролиз К. до b-аланина и гистидина. К. синтезируют из хлорангидрида N-фталил-b-аланина и гистидина (выход ок. 27%) или выделяют из измельченных мышц экстрагированием водой при 60 °С с послед. осаждением К. из безбелкового фильтрата солями Ag и Ва. Для определения К. используют бумажную и колоночную хроматографию (в отсутствие анзерина) или фотометрируют при 640 нм продукт его взаимод. с о-фталевым альдегидом. Последний метод используют для суммарного определения анзерина и К. Р-ры К. с концентрацией 10-20 мМ в экспериментах на животных оказались эффективными для лечения старческой катаракты и при заживлении послеоперационных ран. По зарубежным данным, м.б. использован для ускорения заживления ран в стоматологич. хирургии. Лит.: Мешков Н. П., "Успехи биологической химии", 1964, № 6, с. 86-107; Северин С. Е., Болдырев А. А., Дупин А. М., "Вопросы медицинской химии", 1984, № 3, с. 32-36; Nagai К., Yamane Т., "Heterocycles", 1978, v. 10, p. 277-347; "Comparative Biochemistry and Physiology", 1983, v. 74B, № 3, p. 623-26; "Biochemistry International", 1987, v. 15, № 6, p. 1105-15. C. E. Северин.


