СУЛЬФОКИСЛОТЫ (сульфоновые
к-ты), соед. общей ф-лы RSO3H, где R-Alk, Аr, гетероциклич. радикал.
Классифицируют С. в зависимости от природы R, наличия заместителей и кол-ва
групп SO3H.
С. называют, добавляя к
названиям соединения-основы окончание "сулъфокислота" (сульфоновая
к-та), напр. 4-пиперидинсульфокислота. Если в соединении присутствует другая
группа, имеющая приоритет, к названиям соединения-основы добавляют префикс "сульфо",
напр. n-сульфобензойная кислота. Некоторые С. имеют тривиальные названия.
Сулъфогруппа имеет тетраэдрич.
строение. В сульфонат-анионе 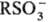 для всех связей S—О длина 0,139 нм, угол OSO
~ 109°; для ароматич. соединений константы Гаммета sмета
0,38, sпара 0,58.
для всех связей S—О длина 0,139 нм, угол OSO
~ 109°; для ароматич. соединений константы Гаммета sмета
0,38, sпара 0,58.
В ИК спектрах С. присутствуют
характеристические полосы в области 1340-1350 и 1150-1160 см-1, соответствующие
асимметрическим и симметрическим валентным колебаниям группы SO2.
В УФ области С. не поглощают. В спектре ПМР хим. сдвиг (d) протона сульфогруппы
11-12 м.д.
С. мало распространены
в природе. Из алифатических С. выделены таурин NH2CH2CH2SO2OH
и цистеиновая к-та NH2CH(CH2SО2ОH)CООH-метаболиты
обмена в-в животных; из ароматических-6-амино-1 -карбокси-10-метил-3-сульфофеназин
(аэругинозин В).
Низшие алкансульфокислоты-
низкоплавкие кристаллич., сильно гигроскопичные в-ва, по кислотности близки
к H2SO4. Наиб. сильная-трифторметансульфокислота (сравнима
с фторсульфоновой к-той).
С. обладают всеми характерными
св-вами кислот: образуют соли и эфиры (сульфонаты), галогенангидриды
(сульфогалогениды), ангидриды, амиды и т.д. При восстановлении С. или сульфохлоридов
цинковой пылью образуются сульфиновые кислоты RS(O)OH, при использовании сильных
восстановителей или в кислой среде-тио-лы RSH.
С. присоединяются по кратным
связям алкенов, алкинов, алленов и др., напр.:
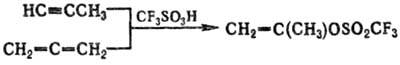
Для ароматических С. характерны
р-ции обмена сульфогруппы на др. функц. группы, напр.:
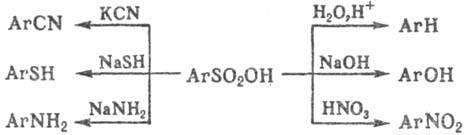
Получают С. 4 осн. методами.
1) Сульфирование органических
соединений. В качестве сульфирующих агентов применяют H2SO4,
олеум, SO3 или его комплексы с пиридином, диоксаном и др., а также
ClSO2OH. Наиболее легко сульфируются активированные гетероароматические
соединения. Важнейшее практическое значение имеет сульфирование ароматических
углеводородов.
При действии сульфирующих
агентов на алифатич. альдегиды, кетоны, карбоновые к-ты и их производные суль-фогруппа
направляется в a-положение, при действии на олефины образуются алкенсульфокислоты
и сультоны, при действии на ацетилен-алкинсульфокислоты наряду с др. продуктами,
напр.:
RCH2COX + SO3
: RCH(SO2OH)COX X = H, OH, R', OR', NR'2
и др.
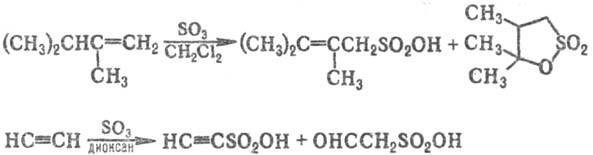
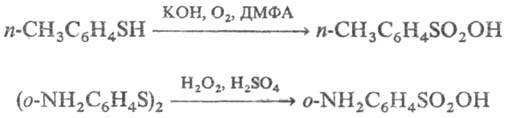
2) Окисление тиолов, сульфидов,
ксантогенатов, тиоциа-натов и т.д. В качестве окислителей используют HNO3,
Н2О2, оксиды азота, пероксикислоты, КМnО4,O3,O2,
напр.:
3) Сульфоокисление и сульфохлорирование,
как правило, алифатич. углеводородов:
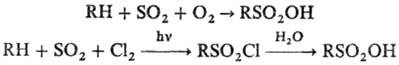
Р-ции идут по свободнорадикальному
механизму. Из вы-сокомол. алканов образуются смеси продуктов; эти процессы используют
гл. обр. в пром-сти.
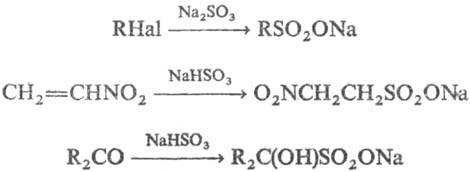
4) Нуклеоф. замещение и
присоединение к кратным связям с участием сульфит-иона. Нуклеоф. атаке могут
подвергаться алкил- и арилгалогениды, оксираны, активир. алкены, ароматич. соед.,
карбонилсодержащие соед., напр.:
Неактивир. алкены и алкины
реагируют с сульфит-ионом в условиях свободнорадикального присоединения.
Качеств. определение С.
основано на взаимод. с NH2OH с образованием сульфогидроксамовой к-ты
RSO(OH)NOH и далее с СН3СНО; при добавлении РеСl3 р-р
окрашивается в темно-красный цвет, переходящий в фиолетовый цвет. Для количеств.
определения используют физ.-хим. методы, а также титрование р-рами щелочей и
осаждение в виде солей тяжелых металлов.
Ароматические С.-полупродукты
в произ-ве фенолов, нафтолов, красителей, лек. ср-в (гл. обр. сульфамидных препаратов),
ионообменных смол, дезинфицирующих ср-в (моно- и дихлорсульфамидов). Техн. смесь
метан-, этан-и пропансульфокислот используют в качестве р-рителя, а также катализатора
этерификации, ацилирования, нитрования, нитрозирования и др. процессов. Соли
алкансуль-фокислот-моющие ср-ва, ПАВ, эмульгаторы, флотореаген-ты, присадки
к техн. маслам, ингибиторы коррозии и т.п.
См. также Метансульфокислота,
Бензолсульфокислоты, Нафталинсульфокислоты, Нафтолсульфокислоты, Толуол-сульфокислоты.
Лит.: Джильберт
Э. Е., Сульфирование органических соединений, пер. с англ., М., 1969; Общая
органическая химия, пер. с англ., т. 5, М., 1983, с. 508-18. А.Ф.Елеев.


