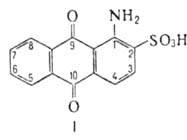
АМИНОАНТРАХИНОНСУЛЬФОКИСЛОТЫ. Наиб. практич. значение имеют 1-аминоантрахинон-2-сульфокислота
(1,2-А., ф-ла I), 1-амино-4-бромантрахинон-2-сульфокислота (бромаминовая
к-та, БАК; в ф-ле I в положении 4 - заместитель Вг), 1-аминоантрахинон-5-сульфокислота
(1,5-А.) и ее N-алкилзамещенные. 1,2-А. и БАК в сухом виде - светло-желтые
кристаллы; их Na- или К-соли - оранжевые; 1,5-А. - красно-коричневые, а
соответствующие ее соли - фиолетовые. А. не имеют характерных т-р плавления;
раств. в воде, ДМФА, умеренно - в спирте, плохо - в других орг. р-рителях.
В видимой области спектра максимумы поглощения в области 470-485 нм (водные
растворы).
А. - сильные к-ты. Образуют гидрохлориды, амиды и эфиры. В 1,2-А. и БАК сульфогруппа затрудняет ацилиро-вание и алкилирование аминогруппы. В 1,5-А. аминогруппа вступает в р-ции, характерные для 1-аминоантрахинона.
При действии одного эквивалента Вr2 на 1,2-А. образуется БАК, при действии двух эквивалентов-1-амино-2,4-дибромантрахинон. 1,5-А. с Вr2 последовательно образует 1-амино-2-бром- и 1-амино-2,4-дибромантрахинон-5-сульфокислоту. При нагр. 1,2-А. со щелочным р-ром Na2S2O4 происходит элиминирование сульфогруппы, а в случае БАК - и галогена с образованием 1-аминоантрахинона. При аминолизе 1,2-А. превращается в 1,2-диаминоантрахинон. 1,5-А. легко обменивает сульфогруппу на амино-, алко-кси- и арилоксигруппы, напр. нагревание в спиртовых р-рах щелочей приводит к 1-амино-5-алкоксиантрахинону-промежут. продукту в синтезе 1-амино-5-гидроксиантрахинона. Диазотирование аминогруппы в среде конц. H2SO4 лежит в основе количеств, определения А.
Важнейшая р-ция БАК, широко используемая в промети, - взаимод. с аминами
в присут. каталитич. кол-в соединений Си, напр. CuCl, (СН3СОО)2Си,
и слабых оснований (NaHCO3, CH3COONa), приводящее
к 1-амино-4-арил(алкил)аминоантрахинон-2-сульфокислотам (в ф-ле I в положении
4-заместители NHAr или NHAlk). Последние - светопрочные кислотные красители
синего цвета или промежут. продукты в синтезе дисперсных, активных, катионных
красителей для крашения в массе и более сложных кислотных красителей. При
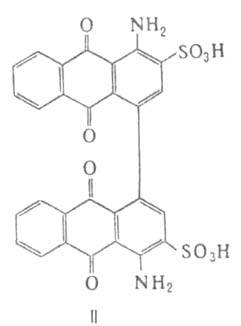
нагр. БАК в слабокислой среде в присут. соединений Сu в результате биарильной
конденсации образуется 1,1-бис-(4-аминоантрахинон-3-сульфокислота) (ф-ла
II)-промежут. продукт в синтезе красного пигмента.
В пром-сти 1,2-А. и БАК получают взаимод. 1-аминоантрахинона с хлорсульфоновой к-той в сухом нитробензоле или полихлоридах. Образующаяся в начале р-ции соль амина при 130°С перегруппировывается в 1,2-А.; реакционную смесь разбавляют водой, отгоняют р-ритель с паром или отделяют водный слой, содержащий 1,2-А., из к-рого ее высаливают добавлением NaCl. 1,2-А. используют гл. обр. для получения БАК и обычно без выделения бромируют Вr2 в водном р-ре или суспензии при рН 5,5-6,5 и 5-15 °С. 1,2-А. получают также сулъфированием 1-аминоантрахинона в олеуме в присут. Na2SO4 или Н3ВО3.
1,5-А. и ее N-алкилзамещенные получают частичным аммонолизом антрахинон-1,5-дисульфокислоты в присут. окислителей (напр., м-нитробензолсульфокислоты).
В лаборатории 1,5-А., а также изомерные 1,6-, 1,7-, 1,8-А. получают восстановлением соответствующих 1-нитроантрахинонсульфокислот водным р-ром Na2S при кипении. 1,5-А. и ее N-алкилзамещенные-промежут. продукты в синтезе кислотных и активных красителей.
Лит.: Ворожцов Н. Н., Основы синтеза промежуточных продуктов
и красителей, 4 изд., М., 1955; Горелик М. В., Химия антрахинонов и их
производных, М., 1983. С.И.Попов.


