ОКСАЗОЛИНЫ (дигидрооксазолы),
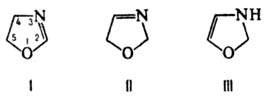
мол.м. 71,09. Различают 2-, 3- и 4-О. (ф-лы соотв. I-III). Наиб. практич. значение
имеют замещенные производные 2-О.; 3- и 4-О. изучены мало. О. и их замещенные
- бесцв. жидкости или кристаллы с запахом пиридина (см. табл.); раств. в воде
и орг. р-рите-лях. О.-слабые основания; для 2-О. рКа 5,5.
2-О. обладают св-вами циклич.
имшоэфиров. Большинство замещенных 2-О. довольно устойчивы к действию
горячей воды, многие из них перегоняются с водяным паром; незамещенный 2-О.
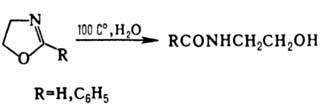
в этих условиях быстро гидролизуется в N-(2-гидроксиэтилен)формамид, 2-фенил-2-оксазолин
при продолжит. кипячении превращ. в N-(2-гидроксиэтил)бензамид:
СВОЙСТВА НЕКОТОРЫХ ОКСАЗОЛИНОВ
|
Заместитель |
Мол. м. |
Т. пл., °С |
Т. кип., °С/мм
рт.ст. |
||
|
|
2-Оксазолины |
|
|||
|
Незамещенный |
71,09 |
_ |
98* |
||
|
2-Метил- |
85,10 |
_ |
108-110 |
||
|
2-Фенил- |
147,17 |
_ |
117-120/5 |
||
|
2-(2-Фурил)- |
137,13 |
82-83 |
- |
||
|
2-Трихлорметил-4,4-диметил-2,5-Дифенил- |
216,49 223,26 |
58-59 |
125-127/0,1 |
||
|
2-Аллиламино- |
112,15 |
- |
1,05/1,0 |
||
|
|
3-Оксазолины |
|
|||
|
4-Амино-2,2,5,5-тетракис
(трифторметил)- |
379,11 |
130-132 |
- |
||
|
4-Этокси-2,2,5,5-тетракис
(трифторметил)- |
372,14 |
- |
136 |
||
* d2020
1,075
С сильными к-тами 2-О.
образуют неустойчивые соли, к-рые при нагр. до т-ры плавления или под действием
Н2О разлагаются с раскрытием цикла, напр.:
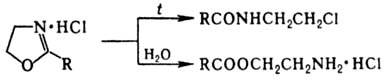
Кислотный или щелочной
гидролиз 2-О. происходит с раскрытием цикла по связи О—С-2, р-ции с уксусным
ангидридом или фенолом-с разрывом связи О—С-5:
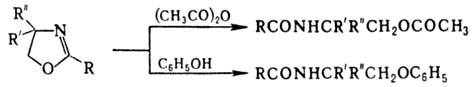
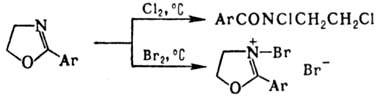
Хлорирование на холоду
2-арилпроизводных протекает с раскрытием цикла, бромирование в аналогичных условиях-без
раскрытия, напр.:
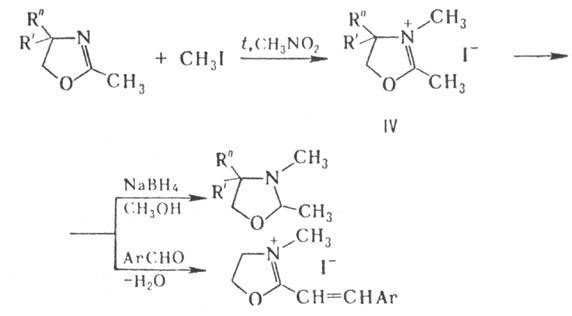
С алкилгалогенидами замещенные
2-О. образуют реак-ционноспособные соли оксазолиния (напр., ф-лы IV); эти соед.
легко восстанавливаются под действием NaBH4 до производных оксазолидина
и конденсируются с ароматич. альдегидами, напр.:
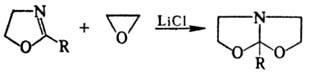
С этиленоксидом в присут.
LiCl 2-замещенные 2-О. образуют 5-замещенные 1-аза-4,6-диоксабицикло[3.3.0]октана:
В условиях катионной полимеризации
при нагр. (60-70 °С) в присут. SnCl4, эфирата BF3,
HClO4 и др. 2-замещенные 2-О. полимеризуются с раскрытием цикла по
связи О—С-5 в N-ацилзамещенные полиэтиленимины с мол.м. 3500-100000.
В аналогичных условиях 2-алкенил-2-оксазолины образуют полимеры, содержащие
в цепи фрагменты 2-О.; 2-изопропенил-2-оксазолины образуют сополимеры с бутил-акрилатом
или метилметакрилатом.
Получают 2-О. и его замещенные
конденсацией 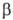 -амино-спиртов
с карбоновыми к-тами, сложными эфирами, имино-эфирами (выход 90-95%), амидинами
и др., напр.:
-амино-спиртов
с карбоновыми к-тами, сложными эфирами, имино-эфирами (выход 90-95%), амидинами
и др., напр.:
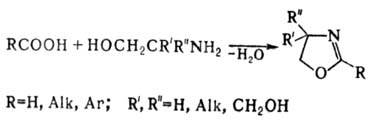
Др. методы синтеза 2-О.:
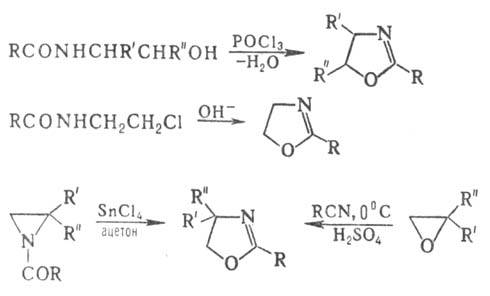
Замещенные 3-О. получают
нагреванием а-гидроксикето-нов с NH3 в уксусной к-те или ароматич.
альдегидами в присут. NH4Cl:
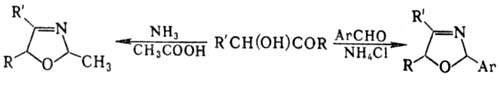
Замещенные 2-О., гл. обр.
2-алкил-4,4-диалкилпроизвод-ные,-присадки к топливам и маслам, антистатики для
полиолефинов и текстильных изделий, ингибиторы коррозии (напр., 2-гептадецил-4,4-диметил-2-О.),
стабилизаторы для ПВХ, пластификаторы каучуков и ВВ, фотосенсибилизаторы (напр.,
2,4-диметил-4-ацетилокси-2-О.), антивспенива-тели, вулканизирующие агенты и
т.д. Соли 2-алкил-2-О. (R = С9-С17) и орг. к-т-катионные
ПАВ и защитные покрытия для металлов (наиб. эффективны соли рицинолевой к-ты).
Нек-рые производные 2-О. проявляют биол. активность [напр., антибиотик хлорамфеникол
- 2-дихлорметил-4-гидроксиметил-5-(4-нитрофенил)-2-О. и 2-алкил(арил)-4,4-диметил-2-О.];
N-замещенные 2-амино-2-О. оказывают действие на центр, нервную систему; 2-замещенные
4-метил-4-гидроксиметил-2-О.-регуляторы роста растений.
Лит.: Гетероциклические
соединения, под ред. Р. Эльдерфилда, пер. с апгл., т. 5, М., 1961, с. 302; Frump
J. A., "Chem. Rev.", 1971, v. 71, № 5, p. 483-505.
P. А. Караханов, В.
И. Келарев.


