УГЛЕРОД ТЕХНИЧЕСКИЙ
(сажа), продукт термич. разложения углеводородов. См.
Технический углерод. УГЛЕРОДА ДИОКСИД (углекислый газ, угольный ангидрид)
CO2, мол. м. 44,01; бесцв. газ с кисловатым запахом и вкусом. Молекула
CO2 имеет линейную конфигурацию, длина связи С — О в своб. молекуле
0,113 нм, в твердом У. д. 0,105 HM. Тройная точка: -56,6 0C, 0,52
МПа; tкрит 31,3 0C, pкрит7,36
МПа; т.возг. -78,5 0C (0,1 МПа). Для газа: плотн. 1,9768 г/л (0 0C,
0,1 МПа); 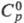 34,57 Дж/(моль·К);
34,57 Дж/(моль·К);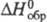 -393,51 кДж/моль;
-393,51 кДж/моль;
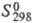 213,67 Дж/(моль·К);
213,67 Дж/(моль·К);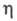 1,39·
10-5 Па·с (0 0C, 1 МПа).
1,39·
10-5 Па·с (0 0C, 1 МПа).
При 20 0C и
давлении 5,7 МПа У. д. сжижается в бесцв. жидкость; плотн. 0,925 кг/дм3
(0 0C, 3,554 МПа); 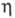 8,5·I0-5 Па·с (10 0C, 5,7 МПа);
8,5·I0-5 Па·с (10 0C, 5,7 МПа); 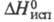 5,27 кДж/моль (6,34 МПа). При нормальном давлении и т-ре -78,5 0C
У. д. кристаллизуется в белую снегоподобную массу; кристаллич. решетка кубич.
гранецентрированная (а = 0,563 нм, z = 4, пространств, группа
Pa3); плотн. 1,56 г/см3 (-78,5 0C).
5,27 кДж/моль (6,34 МПа). При нормальном давлении и т-ре -78,5 0C
У. д. кристаллизуется в белую снегоподобную массу; кристаллич. решетка кубич.
гранецентрированная (а = 0,563 нм, z = 4, пространств, группа
Pa3); плотн. 1,56 г/см3 (-78,5 0C).
У. д. термически весьма
устойчив; диссоциация 2CO2 2CO + O2
начинается ок. 1200 0C; при 2600 0C распадается ок. 50%,
а при 2800 0C - ок. 75% CO2. Р-римость CO2
в воде при нормальном давлении, мл в 100 мл: 171 (0 0C), 102 (15
0C), 66 (30 0C), 36 (60 0C). В коллоидных водных
р-рах орг. B-B р-римость CO2 значительно выше из-за его адсорбции
на коллоидных частицах: Жидкий У. д. хорошо раств. в эфире и низших спиртах,
но почти не растворяет к.-л. твердые в-ва. С водой У. д. образует угольную
кислоту.
2CO + O2
начинается ок. 1200 0C; при 2600 0C распадается ок. 50%,
а при 2800 0C - ок. 75% CO2. Р-римость CO2
в воде при нормальном давлении, мл в 100 мл: 171 (0 0C), 102 (15
0C), 66 (30 0C), 36 (60 0C). В коллоидных водных
р-рах орг. B-B р-римость CO2 значительно выше из-за его адсорбции
на коллоидных частицах: Жидкий У. д. хорошо раств. в эфире и низших спиртах,
но почти не растворяет к.-л. твердые в-ва. С водой У. д. образует угольную
кислоту.
У. д. обладает св-вами
кислотных оксидов, взаимод. с оксидами и гидроксидами щелочных и щел.-зем. металлов,
давая карбонаты. При высокой т-ре CO2 окисляет сильно электро-положит.
металлы (К, Mg, Zn и др.), напр.: 2Mg + CO2 2MgO + С. При пропускании
CO2 над раскаленным углем образуется углерода оксид (р-ция
Будуара): CO2 + С
2MgO + С. При пропускании
CO2 над раскаленным углем образуется углерода оксид (р-ция
Будуара): CO2 + С
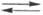 2CO,
эта р-ция очень важна в металлургии. О р-циях с орг. в-вами см. Карбоксилирование.
2CO,
эта р-ция очень важна в металлургии. О р-циях с орг. в-вами см. Карбоксилирование.
В технике У. д. получают
при горении углерода и орг. B-B, как побочный продукт при обжиге известняка
(образующийся при этом CO2 сильно загрязнен азотом), выделением из
коксового газа, а также из дымовых газов обычных котельных установок. Пром.
значение имеет также У. д., образующийся при спиртовом брожении. В нек-рых местностях
для добычи CO2 используют прир. источники газа и сильно минерализованные
воды, пересыщенные У. д. В лабораториях У. д. получают разложением CaCO3,
NaHCO3 или Na2CO3 соляной либо серной к-той.
Для произ-ва жидкого У. д. используют газ с содержанием CO2 выше
95%. После сжатия и охлаждения жидкий CO2 разливают в стальные баллоны
серого цвета. Твердый У. д. ("сухой лед") получают частичным испарением
жидкого CO2.
У. д. содержится в атмосфере
(0,03% по объему), морской воде (ок. 90 г в 1 м3), водах минер. источников
(особенно вблизи вулканов), литосфере в форме минералов - карбонатов (кальцит,
доломит и др.). У. д. образуется при горении и гниении орг. B-B, сжигании топлива,
при дыхании животных и человека, ассимилируется растениями, играя важную роль
в фотосинтезе.
У. д. используют в пищ.
пром-сти в произ-ве сахара, пива, газированных вод, шипучих вин, в медицине
для приготовления углекислых ванн, для тушения пожаров, в качестве нагнетающего
газа для перекачки огнеопасных жидкостей, для консервации пищ. продуктов (CO2
не поддерживает жизнедеятельность бактерий и плесеней), обогащения воздуха в
теплицах (способствует росту растений и повышению урожайности), как пропеллент
в бытовой химии. Твердый У. д.-хладагент, к-рый дает больший охлаждающий эффект,
чем водяной лед, испаряется без остатка и не вызывает коррозии оборудования.
У. д. применяют для произ-ва мочевины [CO2+
2NH3 H2COONH4
H2COONH4  CO(NH2)2
+ H2O], соды по методу Сольвэ (NaCl + NH3 + CO2
+ H2O
CO(NH2)2
+ H2O], соды по методу Сольвэ (NaCl + NH3 + CO2
+ H2O
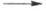 NaHCO3
+ NH4Cl), метанола (CO2 + 3H2
NaHCO3
+ NH4Cl), метанола (CO2 + 3H2
 CH3OH
+ H2O), гидроксикарбоновых к-т (напр., салициловой), для очистки
рассолов NaCl.
CH3OH
+ H2O), гидроксикарбоновых к-т (напр., салициловой), для очистки
рассолов NaCl.
При концентрации У. д.
в воздухе 0,25-1% у человека изменяется ф-ция дыхания и кровообращения, при
2,5-5% наблюдается головная боль, раздражение верх, дыхат. путей и др., при
7% учащается сердцебиение, появляются рвота, головокружение и др. При высоких
концентрациях У. д. в воздухе наступает смерть от остановки дыхания (при 20%
через неск. секунд). Отравления У. д. возможны при очистке бродильных чанов
и цистерн для хранения вина, винных бочек, на складах зерна, в овощехранилищах
и силосных башнях, в погребах с гнилым и проросшим картофелем (вплоть до смертельного
исхода), при очистке канализац. и водопроводных труб, при работе с сухим льдом
и др.
Я. А. Калашников.


