ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ,
величина,
характеризующая способность атома к поляризации ковалентных связей. Если
в двухатомной молекуле А — В образующие связь электроны притягиваются к
атому В сильнее, чем к атому А, то атом В считается более электроотрицательным,
чем А.
Л. Полинг предложил (1932) для количеств.
характеристики Э. использовать термохим. данные об энергии связей А—А,
В — В и А — В - соотв. ЕАА, Евв и ЕАВ.
Энергия
гипотетической чисто ковалентной связи А — В (Еков) принимается
равной среднеарифметич. или среднегеометрич. значению величин
EAA
и ЕВВ.
Если Э. атомов А и В различны, то связь
А — В перестает быть чисто ковалентной и энергия связи ЕАВ
станет больше Ековна величину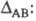
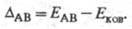
Чем больше различие Э.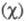 атомов А и В, тем больше величина
атомов А и В, тем больше величина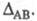 Используя эмпирич. ф-лу
Используя эмпирич. ф-лу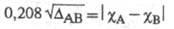 (множитель 0,208 возникает при переводе значений энергии из ккал/моль в
эВ) и принимая для атома водорода произвольное значение Э.
(множитель 0,208 возникает при переводе значений энергии из ккал/моль в
эВ) и принимая для атома водорода произвольное значение Э.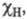 равное 2,1, Полинг получил удобную шкалу относит. числовых значений Э.,
часть к-рых приведена в табл. Наиб. электроотрицателен самый легкий из
галогенов - F, наименее - тяжелые щелочные металлы.
равное 2,1, Полинг получил удобную шкалу относит. числовых значений Э.,
часть к-рых приведена в табл. Наиб. электроотрицателен самый легкий из
галогенов - F, наименее - тяжелые щелочные металлы.
Для количеств. описания Э., помимо термохим.
данных, используют также данные о геометрии молекул (напр., метод Сандерсона),
спектральные характеристики (напр., метод Горди).


